某温度下,将3mol A和2mol B充入一密闭容器中,发生下列反应:aA(气)+B(气)?C(气)+D(气),5分钟后达到平衡状态,已知一定温度下,各物质的平衡浓度符合下列关系:[A]a[B]=[C][D],若在温度不变的条件下,将上述容器的体积扩大为原来的10倍,发现A的转化率不发生变化,则B的转化率为( )
| A、60% | B、40% |
| C、24% | D、4% |
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表下列说法错误的是( )
| 物质 | X | Y | Z |
| 初始浓度/mol?L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol?L-1 | 0.05 | 0.05 | 0.1 |
| A、反应达到平衡时,y的转化率为75% |
| B、反应可表示为X+3Y?2Z,其平衡常数为1600 |
| C、增大压强使平衡向生成Z的方向移动,平衡常数不变 |
| D、改变温度但不可以改变此反应的平衡常数 |
已知2SO2(g)+O2(g)?2SO3(g)△H=-a kJ?mol-1(a>0).恒温恒容下,在10L的密闭容器中加入0.1mol SO2和0.05mol O2,经过2min达到平衡状态,反应放出热量x kJ下列判断正确的是( )
| A、反应放出热量x=0.05a |
| B、反应达到平衡状态时,2v(SO2)消耗=v(O2)生成 |
| C、若恒温恒压下,在10L的密闭容器中加入0.1mol SO2和0.05mol O2,平衡后反应放出的热量y kJ,则y<x |
| D、升高温度,平衡常数变小 |
可逆反应①X(g)+2Y(g)?2Z(g)、②2M(g)?N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板.反应开始和达到平衡状态时有关物理量的变化如图所示:下列判断正确的是( )


| A、反应①的逆反应是放热反应 | ||
| B、达平衡(Ⅰ)时体系的压强与反应开始时体系的压强之比为11:10 | ||
C、达平衡(Ⅰ)时,X的转化率为
| ||
| D、在平衡(Ⅰ)和平衡(Ⅱ)中,M的体积分数相等 |
 某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2.
某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2.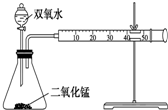 某化学实验小组为确定过氧化氢分解的最佳催化条件,用如图装置进行实验,反应物用量和反应停止的时间数据如下表:
某化学实验小组为确定过氧化氢分解的最佳催化条件,用如图装置进行实验,反应物用量和反应停止的时间数据如下表: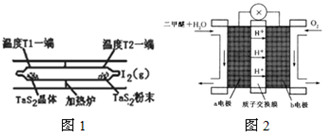
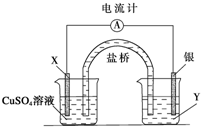 根据下列氧化还原反应2FeCl3+Cu═2FeCl2+CuCl2设计一个原电池:
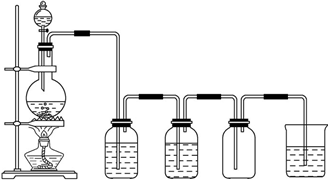
根据下列氧化还原反应2FeCl3+Cu═2FeCl2+CuCl2设计一个原电池: 镁在空气中燃烧除生成MgO外,还可能生成Mg3N2.某校化学兴趣小组的同学利用镁在空气中燃烧后的固体(不含单质)进行实验,探究其组成.
镁在空气中燃烧除生成MgO外,还可能生成Mg3N2.某校化学兴趣小组的同学利用镁在空气中燃烧后的固体(不含单质)进行实验,探究其组成.