取一定量的镁、铝合金,用足量盐酸溶解后,再加入过量的氢氧化钠溶液,然后滤出沉淀物,加强热灼烧最后得到白色粉末,干燥后称量与原合金的质量相等,则合金中镁的质量百分含量是( )
| A、20% | B、40% |
| C、60% | D、无法计算 |
下列物质转化在给定的条件下能实现的是( )
①Al2O3
NaAlO2(aq)
Al(OH)3
②S
SO3
H2SO4
③石油化工采用银作催化剂,可以实现一步完成:2CH2=CH2+O2
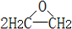
④Fe2O3
FeCl3(aq)
无水FeCl3
⑤MgCl2(aq)
Mg(OH)2
MgO
⑥NH3
NO
HNO3.
①Al2O3
| NaOH(aq) |
| △ |
| CO2 |
②S
| O2/点燃 |
| H2O |
③石油化工采用银作催化剂,可以实现一步完成:2CH2=CH2+O2
| Ag |
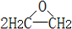
④Fe2O3
| HCl(aq) |
| △ |
⑤MgCl2(aq)
| 石灰乳 |
| 煅烧 |
⑥NH3
| O2 |
| O2,H2O |
| A、①②③④ | B、①③④⑥ |
| C、①③⑤⑥ | D、②④⑤⑥ |
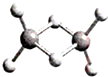 近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物Al2H6的球棍模型如图所示,它的熔点为150℃,燃烧热极高.下列说法错误的是( )
近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物Al2H6的球棍模型如图所示,它的熔点为150℃,燃烧热极高.下列说法错误的是( )| A、氢铝化合物与水反应生成氢氧化铝和氢气 |
| B、Al2H6中含有离子键和极性共价键 |
| C、氢铝化合物可能成为未来的储氢材料和火箭燃料 |
| D、氢铝化合物中可能存在组成为AlnH2n+2的物质(n为正整数) |
在以Al2O3为原料制备Al(OH)3可以使用如下路线:Al2O3
AlCl3
Al(OH)3,则X最适宜用的试剂( )
| HCl |
| X |
| A、NH3?H2O |
| B、CO2 |
| C、NaOH |
| D、HCl |
化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A、明矾水解生成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
| B、高温电解Al2O3可制得金属铝 |
| C、MgO的熔点很高,可用于制作耐高温材料 |
| D、根据冷的浓硫酸可以用铝质容器储存的事实,说明常温下铝不会与浓硫酸发生反应 |
往AlCl3溶液中逐滴滴入NaOH溶液至过量,可观察到的现象是( )
| A、有白色絮状沉淀产生,且不溶解 |
| B、先无现象,后有白色絮状沉淀 |
| C、一直无明显现象 |
| D、先有白色絮状沉淀,后又溶解 |
由MgO、Al2O3、SiO2、Fe2O3组成的混合粉末.现取一份该混合粉末试样进行实验,首先将其溶于过量的盐酸,过滤后,得到沉淀X和滤液Y.下列叙述正确的是( )
| A、从组成看,其成分皆是碱性氧化物 |
| B、溶液Y中的阳离子主要是Mg2+、Al3+、Fe2+、H+ |
| C、沉淀X的成分是SiO2 |
| D、在溶液Y中加入过量的氨水,过滤得到的沉淀的成分是Fe(OH)3和Mg(OH)2 |
取少量MgO、Al2O3、SiO2、Fe2O3的混合粉末,加入过量盐酸,充分反应后过滤,得到固体X和滤液Y.下列叙述正确的是( )
| A、上述四种氧化物对应的水化物中,至少有三种是碱性氧化物 |
| B、将固体X加入氢氟酸中,X会溶解 |
| C、滤液Y中的阳离子只有Mg2+、Al3+、Fe3+三种 |
| D、滤液Y中加入过量氨水,所得沉淀为Fe(OH)3和Mg(OH)2 |
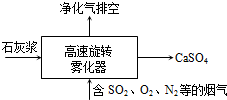 硫元素有多种化合价,可形成多种化合物.
硫元素有多种化合价,可形成多种化合物.