将c(H+)=10-2mol?L-1的醋酸和盐酸分别稀释100倍,稀释后两种溶液的c(H+)分别为a和b,则a和b的关系为( )
| A、a>b | B、a<b |
| C、a=b | D、无法判断 |
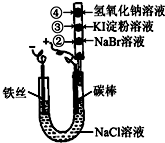 某化学兴趣小组按如图所示的装置进行实验,玻璃管内装有滴有不同溶液的白色棉球.实验过程中,两极均有气体生成.则下列说法错误的是( )
某化学兴趣小组按如图所示的装置进行实验,玻璃管内装有滴有不同溶液的白色棉球.实验过程中,两极均有气体生成.则下列说法错误的是( )| A、碳棒的电极反应式为2Cl--2e-=Cl2↑ | ||||
| B、②处、③处白色棉球分别变为橙黄色、蓝色 | ||||
C、如图X、Y两条线分别表示常见的非金属单质和金属单质(用M表示)与碳棒电解产物单质E在点燃条件下进行化合反应的物质的量之间的关系.写出符合Y线反应的化学方式Mg+Cl2
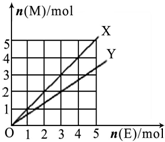 | ||||
| D、在20℃时饱和食盐水的质量分数为26%,当阳极析出1.12L(标准状况下)气体时,Cl-完全放电.试计算要使溶液恢复原状态,需加入3.65gHCl气体 |
对于常温下pH=12的氨水,下列说法正确的是( )
| A、由水电离产生的c(OH-)=10-12mol?L-1 | ||
| B、向溶液中加入适量盐酸使混合液的pH=7,混合液中c(NH4+)>c(Cl-) | ||
| C、等体积pH=12的氨水和pH=12的NaOH溶液可中和等物质的量的HCl | ||
D、用水稀释时,溶液中
|
在醋酸中存在电离平衡:CH3COOH?CH3COO-+H+,要使电离平衡右移且c(H+)增大,应采取的措施是( )
| A、加入NaOH(s) |
| B、加入盐酸 |
| C、加蒸馏水 |
| D、升高温度 |
从海水中提取溴常用的一种工艺涉及以下过程:则正确的步骤为( )
①氧化:用Cl2将海水中的NaBr氧化成Br2;
②将海水浓缩;
③提取:用Cl2将HBr氧化成Br2得到产品;
④富集:用空气和水蒸气将Br2吹入吸收塔与吸收剂SO2水溶液反应生成HBr.
①氧化:用Cl2将海水中的NaBr氧化成Br2;
②将海水浓缩;
③提取:用Cl2将HBr氧化成Br2得到产品;
④富集:用空气和水蒸气将Br2吹入吸收塔与吸收剂SO2水溶液反应生成HBr.
| A、②①③④ | B、①②③④ |
| C、③②①④ | D、②①④③ |
下列物质的制备合理的是( )
①将氯化铝与硫化钾溶液混合后过滤来制备硫化铝
②将过量的铁与氯气加热反应制备氯化亚铁
③在配制的硫酸亚铁溶液常加入一定量的铁粉和硫酸
④铜先氧化成氧化铜,再与硫酸反应来制取硫酸铜
⑤将45mL水加入到盛有5g氯化钠的烧杯中,溶解配制50g质量分数为5%的氯化钠溶液.
①将氯化铝与硫化钾溶液混合后过滤来制备硫化铝
②将过量的铁与氯气加热反应制备氯化亚铁
③在配制的硫酸亚铁溶液常加入一定量的铁粉和硫酸
④铜先氧化成氧化铜,再与硫酸反应来制取硫酸铜
⑤将45mL水加入到盛有5g氯化钠的烧杯中,溶解配制50g质量分数为5%的氯化钠溶液.
| A、只有④ | B、只有②③ |
| C、只有③④ | D、全部 |
化学在生产和日常生活中有着重要的应用.下列说法中不正确的是( )
| A、明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
| B、日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 |
| C、用Al(OH)3制胃酸过多 |
| D、电解AlCl3饱和溶液,可制得金属铝 |
盐酸、醋酸和碳酸氢钠是化学中的常见物质.下列表述正确的是( )
| A、在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO32-和OH- |
| B、NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-) |
| C、CH3COOH溶液中加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D、中和体积与pH值都相同的盐酸和醋酸溶液,所消耗NaOH的物质的量相同 |
从海水中提取镁的工业流程如图所示,下列说法正确的是( )

| A、在实验室进行②的操作需用到坩埚、坩埚钳、玻璃棒、酒精灯 |
| B、步骤⑥电解MgCl2时,阴极产生H2 |
| C、步骤⑤应将晶体置于HCl气体氛围中脱水 |
| D、上述工艺流程中的反应未涉及氧化还原反应 |