X、Y两元素可形成X2Y3型化合物,则X、Y原子基态时价电子的电子排布不可能是( )
| A、X:3d64s2 Y:2s22p4 |
| B、X:2s22p3Y:2s22p4 |
| C、X:3s23p1Y:3s23p4 |
| D、X:3s2Y:3s23p5 |
对于钠原子的第3层电子的p轨道3px、3py、3pz间的差异,下列几种说法中正确的是( )
| A、电子云形状不同 |
| B、原子轨道的对称类型不同 |
| C、电子(基态)的能量不同 |
| D、电子云空间伸展的方向不同 |
某无色透明溶液中,可能含有以下离子中的若干种:K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、CO32-、I-和Cl-,取该溶液进行如下实验:
①溶液滴在pH试纸上,呈红色
②将少许溶液加入铜片和硫酸,有无色气体产生,此气体与空气混合,立即变成红棕色
③取少许溶液滴入BaCl2溶液,则产生白色沉淀
④取实验③中的澄清溶液,滴入AgNO3溶液,产生不溶于稀HNO3的白色沉淀
⑤另取少许溶液,滴入NaOH溶液,有白色沉淀生成,当NaOH过量时,又有部分白色沉淀溶解.根据以上现象判断原溶液中( )
①溶液滴在pH试纸上,呈红色
②将少许溶液加入铜片和硫酸,有无色气体产生,此气体与空气混合,立即变成红棕色
③取少许溶液滴入BaCl2溶液,则产生白色沉淀
④取实验③中的澄清溶液,滴入AgNO3溶液,产生不溶于稀HNO3的白色沉淀
⑤另取少许溶液,滴入NaOH溶液,有白色沉淀生成,当NaOH过量时,又有部分白色沉淀溶解.根据以上现象判断原溶液中( )
| A、②中无色气体中有NO,可能含CO2 |
| B、③中沉淀有BaSO4,可能含BaCO3 |
| C、肯定存在的离子是Al3+、SO42-、NO3-、Mg2+,肯定不存在的离子是 Ba2+、Fe2+、CO32-、I-,不能确定的离子是K+、Cl- |
| D、②中红棕色气体通入水中发生反应的离子方程式为:3NO2+H2O=H++NO3-+2NO |
下列各组指定的元素,不能形成AB2型化合物的是( )
| A、[He]2s22p2和[He]2s22p4 |
| B、[Ne]3s23p4和[He]2s22p4 |
| C、[Ne]3s2和[He]2s22p5 |
| D、[Ne]3s1和[Ne]3s23p4 |
已知某元素的+2价离子的电子排布式为1s22s22p63s23p6,则该元素在周期表中属于( )
| A、第3周期ⅤB族 |
| B、第4周期ⅡB族 |
| C、第4周期Ⅷ族 |
| D、第4周期ⅡA族 |
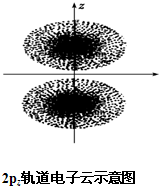 如图是2pz轨道电子云的示意图,请观察图,并判断下列说法中不正确的是( )
如图是2pz轨道电子云的示意图,请观察图,并判断下列说法中不正确的是( )| A、2pz轨道上的电子在空间出现的概率分布是z轴对称 |
| B、点密集的地方表明电子出现的机会多 |
| C、电子先沿z轴正半轴运动,然后在负半轴运动 |
| D、2pz轨道形状为两个椭圆球 |