一定量的混合气体在密闭容器中发生如下反应:mA(g)+nB(g)?pC(g),达平衡后,保持温度不变,将容器的体积缩小为原来的
,当达到新平衡时,测得C的浓度为原来的1.9倍.则下列叙述中正确的是( )
| 1 |
| 2 |
| A、m+n>p |
| B、A的转化率增大 |
| C、平衡逆向移动 |
| D、C的体积百分含量增大 |
在恒温、容积为2L的密闭容器中充入2mol SO2和一定量O2.发生反应2SO2+O2?2SO3,当反应进行到4min时,测得n(SO2)=0.4mol.若反应进行到2min时,容器中SO2的物质的量是( )
| A、等于1.6 mol |
| B、等于1.2 mol |
| C、大于1.6 mol |
| D、小于1.2 mol |
一定条件下,体积为5L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g)Z(g),经60s达到平衡,生成0.3molZ.下列说法正确的是( )
A、将容器体积变为10L,Z的平衡浓度变为原来的
| ||
| B、以X浓度变化表示的反应速率为0.001mol/(L?S) | ||
| C、若升高温度,X的体积分数增大,则该反应的△H>0 | ||
| D、若增大压强,则物质Y的转化率增大 |
 甲、乙、丙、丁四种物质转化关系如图.已知甲是地壳中含量最高的元素组成的单质.
甲、乙、丙、丁四种物质转化关系如图.已知甲是地壳中含量最高的元素组成的单质.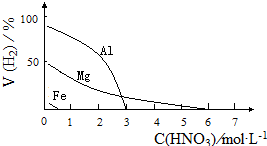 HNO3是一种氧化性的强酸,与金属反应情况多种多样.为探究HNO3性质,某兴趣小组作如下探究:
HNO3是一种氧化性的强酸,与金属反应情况多种多样.为探究HNO3性质,某兴趣小组作如下探究: