取x g铜镁合金完全溶于浓硝酸中,若反应过程中HNO3被还原只生成NO、NO2,收集产生的气体,再通入0.56L氧气(标况),气体恰好可以被水吸收,在合金与HNO3反应后的溶液中加入足量的NaOH溶液可以生成3.9g沉淀,则x等于( )
| A、1.2g | B、2.2g |
| C、3.2g | D、无法计算 |
现有X、Y、Z三种物质,各取40g相混合,完全反应后,得Y 18g,Z 49g,还有W生成.已知W的式量为106,现将22gX和11gY反应,能生成W为( )
①0.5mol ②0.25mol ③53g ④26.5g.
①0.5mol ②0.25mol ③53g ④26.5g.
| A、①③ | B、①④ | C、②④ | D、②③ |
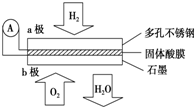 某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见图,电池总反应可表示为:2H2+O2═2H2O,下列有关说法正确的是( )
某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见图,电池总反应可表示为:2H2+O2═2H2O,下列有关说法正确的是( )| A、电子通过外电路从b极流向a极 |
| B、b极上的电极反应式为:O2+2H2O+4e-═4OH- |
| C、每转移0.1 mol电子,消耗标准下1.12 L的H2 |
| D、H+由b极通过固体酸电解质传递到a极 |
已知:2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1 H2(g)+O2(g)═H2O(l)△H=-285.8kJ?mol-1由此可知,在等温下蒸发36g液态水需吸收的热量( )
| A、483.6 kJ |
| B、88 kJ |
| C、285.8 kJ |
| D、44 kJ |
已知热化学方程式:2SO2(g)+O2═2SO3(g)△H=-196.64kJ?mol-1.在某密闭容中充入1mol SO2和足量O2充分反应后,放出热量( )(反应条件相同)
| A、等于98.32kJ |
| B、大于98.32kJ |
| C、小于98.32kJ |
| D、无法判断 |
在指定环境中,下列各组离子一定可以大量共存的是( )
| A、加入铝可以产生H2的溶液中:Al3+、K+、SO42-、Cl- |
| B、在由水电离的c(OH-)=10-14mol?L-1 的溶液中:Fe2+、NH4+、NO3-、Cl- |
| C、在pH=11的溶液中:SO32-、K+、Na+、CO32- |
| D、在酸性溶液中:AlO2-、I一、NO3-、Na+ |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、通入足量CO2后的溶液中:Na+、SiO32-、C6H5O-、CH3COO- | ||
B、
| ||
| C、pH=0的溶液:Al3+、Ag(NH3)2+、Cl-、SO42- | ||
| D、c(ClO-)=1.0 mol?L-1的溶液:Na+、SO32-、S2-、SO42- |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、1.0mol?L-1 KNO3溶液:H+、Fe2+、SCN-、SO42- | ||
B、
| ||
| C、pH=0的溶液:Al3+、Ag(NH3)2+、Cl-、SO42- | ||
| D、c(ClO-)=1.0 mol?L-1的溶液:Na+、SO32-、S2-、SO42- | ||
| E、与铝反应产生H2的溶液中:NO3-、Na+、Cl-、K+ |
 材料的不断发展可以促进社会进步.
材料的不断发展可以促进社会进步.