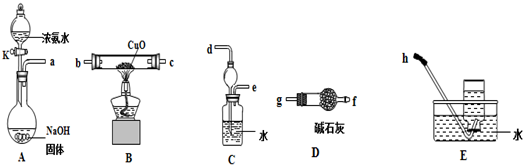
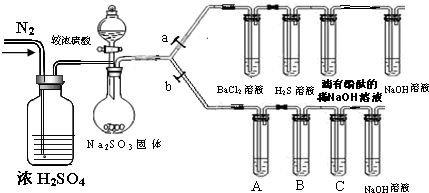
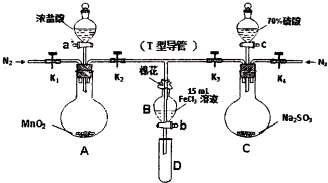
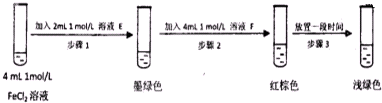
0 131860 131868 131874 131878 131884 131886 131890 131896 131898 131904 131910 131914 131916 131920 131926 131928 131934 131938 131940 131944 131946 131950 131952 131954 131955 131956 131958 131959 131960 131962 131964 131968 131970 131974 131976 131980 131986 131988 131994 131998 132000 132004 132010 132016 132018 132024 132028 132030 132036 132040 132046 132054 203614