已知298K时,Mg(OH)2的容度积常数KKsp=5.6×10-12,MgCO3容度积常数KKsp=6.8×10-6,取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀溶解平衡,测得pH=13.0,则下列说法不正确的是( )
| A、298K时在水中溶解能力Mg(OH)2弱于MgCO3 |
| B、MgCO3悬浊液中加入适量的烧碱溶液可以生成Mg(OH)2沉淀 |
| C、沉淀溶解平衡时溶液中的c(Mg2+)=5.6×10-10mol?L-1 |
| D、298时饱和Mg(OH)2溶液与饱和MgCO3溶液相比前者的c(Mg2+)大 |
下列叙述不正确的是( )
A、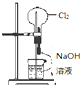 . .挤压胶头滴管后会看到烧瓶中形成喷泉 |
B、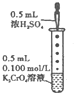 滴加几滴浓H2SO4后,溶液颜色由黄色变为橙色 |
C、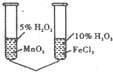 由该实验可以验证催化剂的催化效果 |
D、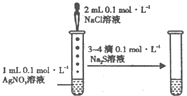 能验证AgCl沉淀可转化为溶解度更小的Ag2S沉淀 |
如表为有关化合物的pKsp,pKsp=-lgKsp.某同学设计实验如下:①向AgNO3溶液中加入适量NaX溶液,得到沉淀AgX;②向①中加NaY,则沉淀转化为AgY;③向②中加入NaZ,沉淀又转化为AgZ.则表中a、b、c的大小关系为( )
| 相关化合物 | AgX | AgY | AgZ |
| pKsp | a | b | c |
| A、a>b>c |
| B、a<b<c |
| C、c<a<b |
| D、a+b=c |

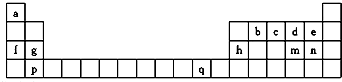
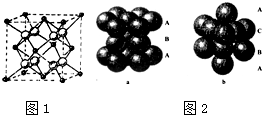
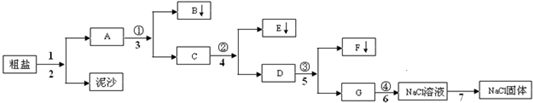
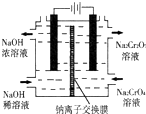 (1)已知在常温常压下:
(1)已知在常温常压下: ),聚丙烯酸钠单体的结构简式是
),聚丙烯酸钠单体的结构简式是