在体积为0.5L的恒容密闭容器中充入1.25mol N2和1.25mol H2,进行反应:N2(g)+3H2(g)?2NH3(g),△H=-92.4kJ?mol-1,在不同温度下达到平衡时测得H2的体积分数如下表所示,下列说法中不正确的是( )
| T/℃ | 200 | 300 | 400 |
| H2的体积分数 | a1 | a2 | 25% |
| A、a1<a2 |
| B、若反应在400℃下进行,则达到平衡时N2的转化率为20% |
| C、若反应在300℃下进行,则达到平衡时反应放出的热量为23.1 kJ |
| D、若反应在200℃下进行,则达到平衡时N2的体积分数为50% |
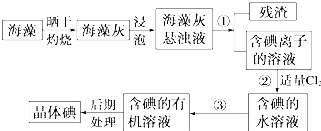
 海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如下:
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如下: