在一定条件下,将3mol A和1mol B两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)?xC(g)+2D(g).2min末该反应达到平衡,生成0.8mol D,并测得C的浓度为0.2mol?L-1.下列判断错误的是( )
| A、x=1 |
| B、2min内A的反应速率为0.3mol?L-1?min-1 |
| C、B的转化率为50% |
| D、若混合气体的平均相对分子质量不变,则表明该反应达到平衡状态 |
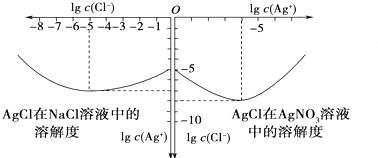
一定温度下,溴化银在水中的沉淀溶解平衡曲线如图,下列说法正确的是( )


| A、向溴化银的浊液中加入溴化钠溶液,溴化银的Ksp减小 |
| B、向c点的溶液中加入0.1mol?L-1AgNO3,则c(Br-)减小 |
| C、升高温度可以实现c点到b点的转化 |
| D、图中b点对应的是不饱和溶液 |
甲烷燃烧的化学方程式为CH4+2O2=CO2+2H2O.常温常压下,将1体积甲烷在3体积氧气中完全燃烧,再将生成的气体恢复到原来的温度和压强.求生成多少体积的二氧化碳?剩余什么气体?它的体积是多少??
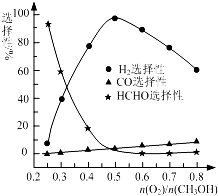 甲醇来源丰富、价格低廉、运输贮存方便,有着重要的用途和应用前景.
甲醇来源丰富、价格低廉、运输贮存方便,有着重要的用途和应用前景.