A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,原子半径按D、E、B、C、A顺序依次减小,B和E同主族.下列推断中不正确的是( )
| A、A、B、E一定在不同周期 |
| B、A、D可能在同一主族 |
| C、C元素的最高价氧化物对应的水化物可能显碱性 |
| D、C和D单质化合可能形成离子化合物 |
某盐溶液中含有K+、Zn2+、Cl-、SO42-四种离子,若n(K+)为0.2mol,n(Zn2+)为0.4mol,n(Cl-)为0.4mol,则SO42-的物质的量为( )
| A、0.3mol |
| B、0.5mol |
| C、0.15mol |
| D、0.2mol |
下列物质分子的几何构型为三角锥形的是( )
| A、CO2 |
| B、P4 |
| C、NH3 |
| D、H2O |
下列说法中正确的是( )
| A、PCl3、NH3、BF3分子中所有原子的最外层电子都满足了8e-稳定结构 |
| B、1mol SiO2 中含有2mol共价键 |
| C、NaCl晶体中与每个Na+距离相等且最近的Na+共有12个 |
| D、原子间通过共价键而形成的晶体一定具有高的熔、沸点及硬度 |
下列叙述正确的是( )
| A、凡是中心原子采取sp3杂化方式成键的分子其几何构型都是正四面体 |
| B、NF3分子的空间构型为三角锥形,中心原子的原子轨道杂化方式为sp3杂化 |
| C、CH2═CH2可用sp杂化轨道来解释 |
| D、CH4分子中的4个C-H键都是氢原子的1s轨道与碳原子的2p轨道形成的s-p σ键 |
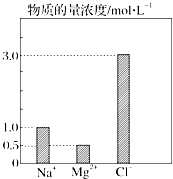 在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示.
在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示.