相同温度,体积均为0.5L的两个恒容容器中发生可逆反应:A(g)+3B(g)═2C(g)△H=-92.6kJ?mol-1,实验测得反应在起始、达到平衡时的有关数据如下表所示 下列叙述不正确的是( )
| 容器编号 | 各物质物质量/ | 达到平衡时体系能量变化 | ||
| A | B | C | ||
| ① | 1 | 3 | 0 | 放热46.3kJ |
| ② | 0.3 | 0.9 | 1.4 | |
| A、达平衡时,两个容器中C的物质的量浓度均为1.0mol?L-1 |
| B、容器①达平衡A转化率是50% |
| C、容器②中达平衡时吸收的热量为18.52kJ |
| D、若起始容器中A、B、C各为0.5mol,则达平衡前υ(正)<υ(逆) |
若在1L蒸馏水中加入1滴(约0.05mL)0.1mol?L-1的NaCl溶液,搅拌均匀后再滴入1滴0.1mol?L-1 AgNO3溶液是否会产生沉淀(已知AgCl的Ksp=1.8×10-10)( )
| A、否 | B、是 |
| C、可能是 | D、以上都不正确 |
 773K时,将等物质的量的H2O与CO至于1L的密闭容器中,发生反应:H2O(g)+CO(g)?H2(g)+CO2(g)△H<0,其CO的转化率如图所示.下列说法中正确的是( )
773K时,将等物质的量的H2O与CO至于1L的密闭容器中,发生反应:H2O(g)+CO(g)?H2(g)+CO2(g)△H<0,其CO的转化率如图所示.下列说法中正确的是( )| A、t1时CO2的浓度大于t2时CO2的浓度 |
| B、773K时,该反应的化学平衡常数为0.75 |
| C、773K时,在上述平衡体系中再充入CO,化学平衡常数减小 |
| D、对上述平衡体系加热,化学平衡常数减小 |
牙齿表面由一层硬的成分为Ca5(PO4)3OH的物质保护,它在唾液中存在下列平衡:Ca5(PO4)3OH?5Ca2++3PO43-+OH-已知Ca5(PO4)3F(s)的溶解度比Ca5(PO4)3OH(s)更小,为了保护牙齿,可采用不同的措施.以下措施中不能保护牙齿的是( )
| A、饮用酸性饮料 |
| B、在牙膏中添加适量的Ca2+离子 |
| C、少吃甜食 |
| D、在牙膏中加入氟化物添加剂 |
 常温下,Ksp(CaSO4)=9×l0-6,常温下CaSO4在水中的沉淀溶解平衡曲线如图.下列判断错误的是( )
常温下,Ksp(CaSO4)=9×l0-6,常温下CaSO4在水中的沉淀溶解平衡曲线如图.下列判断错误的是( )| A、a、c两点均可以表示常温下CaS04溶于水所形成的饱和溶液 |
| B、a点对应的Ksp不等于c点对应的Ksp |
| C、b点将有沉淀生成 |
| D、向d点溶液中加入适量CaCl2固体可以变到c点 |
25℃,石灰浆中存在下列平衡:Ca(OH)2(s)═Ca2+(aq)+2OH-(aq),当向一定量的石灰浆中加入少量生石灰后并恢复到原来的温度,下列说法正确的是( )
| A、溶液中c(Ca2+)增大 |
| B、溶液中溶质的质量分数增大 |
| C、溶液的pH增大 |
| D、溶液中Ca2+离子数目减少 |
下列高聚物必须是由两种不同的单体经加聚反应而生成的是( )
A、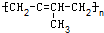 |
B、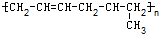 |
C、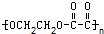 |
D、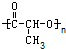 |
在下列溶液中BaSO4溶解度最大是的( )
| A、1mol/L H2SO4溶液 |
| B、0.5mol/L BaCl2溶液 |
| C、0.1mol/L Na2SO4溶液 |
| D、0.2mol/L (NH4)2SO4溶液 |
下表是五种银盐的溶度积常数(25℃),下列有关说法错误的是( )
| 化学式 | AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 溶度积 | 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 5.0×10-13 | 8.3×10-17 |
| A、五种物质在常温下溶解度最大的是Ag2SO4 |
| B、向AgCl的悬浊液中加入0.1mol/L Na2S溶液,则可以生成黑色的Ag2S沉淀 |
| C、外界条件改变时,沉淀溶解平衡也会发生移动 |
| D、常温下,向AgI的悬浊液中加入0.1mol/L NaCl溶液,黄色沉淀变成白色沉淀 |