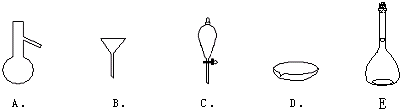
一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验.某研究性学习小组在实验室中配制1mol?L-1的稀硫酸标准溶液,然后用其滴定某未知浓度的NaOH溶液.下列有关说法错误的是( )
| A、实验中所用到的滴定管、容量瓶,在使用前均需要检漏 |
| B、如果实验中需用60 mL的稀硫酸标准溶液,配制时应选用100 mL容量瓶 |
| C、酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,则测得的NaOH溶液的浓度将偏大 |
| D、中和滴定时,将甲基橙滴入待测NaOH溶液中,达到滴定终点时,甲基橙指示剂的颜色由橙色变为黄色 |
下面是某化学研究小组探究外界条件对化学反应速率和化学平衡影响的图象,其中图象和实验结论表达均正确的是( )
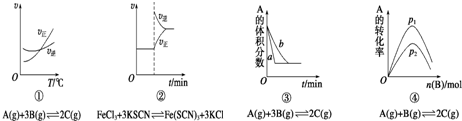

| A、①是其他条件一定时,反应速率随温度变化的图象,正反应△H>0 |
| B、②是在平衡体系的溶液中溶入少量KCl晶体后化学反应速率随时间变化的图象 |
| C、③是在有无催化剂存在下建立的平衡过程图象,b是使用催化剂时的曲线 |
| D、④是一定条件下,向含有一定量A的容器中逐渐加入B时的图象,压强p1>p2 |
在密闭容器中,一定量混合气体发生下列反应:aM(g)+bN(g)?cW(g),达一平衡后,测得M气体的浓度为0.5mol/L.当在恒温下,将密闭容器的体积扩大1倍,再达平衡时,测得M气体的浓度为0.3mol/L.则下列叙述正确的是( )
| A、反应速率增大 |
| B、W的体积分数降低 |
| C、N的转化率提高 |
| D、平衡向右移动 |
为除去括号内杂质,下列有关试剂和操作方法不正确的是( )
| A、苯(苯酚):稀NaOH溶液,分液 |
| B、乙醇(乙酸):KOH溶液,分液 |
| C、乙烷(乙烯):溴水,洗气 |
| D、苯(溴):稀NaOH溶液,分液 |
以下有关实验的叙述中,正确的是( )
| A、利用萃取分液操作分离汽油和CCl4 |
| B、用玻璃棒蘸取待测液,点在润湿的pH试纸上测定其pH |
| C、用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 |
| D、读取滴定管内液体的体积,俯视读数导致读数偏小 |
某溶液中只含有K+、Na+、NO3-、SO42-四种离子(不考虑水的电离)它们的物质的量之比为1:6:3:2,该溶液所含的溶质可能是( )
| A、KNO3、Na2SO4 |
| B、K2SO4、NaNO3、KNO3 |
| C、KNO3、Na2SO4、NaNO3 |
| D、K2SO4、Na2SO4、KNO3 |
如图各种尾气吸收装置中,适合于吸收NH3气体,而且能防止倒吸的有 ( )
A、 |
B、 |
C、 |
D、 |
E、 |
 (1)0.4molNH4ClO4含有氧原子数为
(1)0.4molNH4ClO4含有氧原子数为