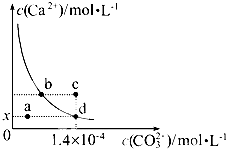
 室温时,CaCO3在水中的溶解平衡曲线如图所示,已知:25℃其溶度积为2.8×10-9,下列说法不正确的是( )
室温时,CaCO3在水中的溶解平衡曲线如图所示,已知:25℃其溶度积为2.8×10-9,下列说法不正确的是( )| A、加入蒸馏水可使溶液由d点变到a点 |
| B、c点时有碳酸钙沉淀生成 |
| C、x数值为2×10-5 |
| D、b点与d点对应的溶度积相等 |
25℃、101kPa 下:
①2Na(s)+1/2O2(g)=Na2O(s)△H1=-414KJ/mol;
②2Na(s)+O2(g)=Na2O2(s)△H2=-511KJ/mol.
下列说法正确的是( )
①2Na(s)+1/2O2(g)=Na2O(s)△H1=-414KJ/mol;
②2Na(s)+O2(g)=Na2O2(s)△H2=-511KJ/mol.
下列说法正确的是( )
| A、25℃、101kPa 下,Na2O2(s)+2 Na(s)=2Na2O(s)△H=-317kJ/mol |
| B、①和②生成等物质的量的产物,转移电子数不同 |
| C、常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| D、①和②产物的阴阳离子个数比不相等 |
已知下列热化学方程式:
①C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
②CO(g)+
O2(g)═CO2(g)△H=-283.0kJ/mol
③2Fe(s)+3CO(g)═Fe2O3(s)+3C(s)△H=-489.0kJ/mol
则4Fe(s)+3O2(g)═2Fe2O3(s)的反应热△H为( )
①C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
②CO(g)+
| 1 |
| 2 |
③2Fe(s)+3CO(g)═Fe2O3(s)+3C(s)△H=-489.0kJ/mol
则4Fe(s)+3O2(g)═2Fe2O3(s)的反应热△H为( )
| A、-1641.0kJ/mol |
| B、+3081kJ/mol |
| C、+663.5kJ/mol |
| D、-2507.0kJ/mol |
实验室中利用复分解反应制取Mg(OH)2.实验数据和现象如下表所示(溶液体积均取用1mL)
关于以上实验的说法正确是( )
| 组别 | 药品1 | 药品2 | 实验现象 |
| Ⅰ | 0.1mol/LNaOH溶液 | 0.1mol/LMgCl2溶液 | 生成白色沉淀 |
| Ⅱ | 0.1mol/L氨水 | 0.1mol/LMgCl2溶液 | 无现象 |
| Ⅲ | 1mol/L氨水 | 1mol/LMgCl2溶液 | 现象Ⅲ |
| Ⅳ | 1mol/L氨水 | 0.1mol/LMgCl2溶液 | 生成白色沉淀 |
| Ⅴ | 0.1mol/L氨水 | 1mol/LMgCl2溶液 | 无现象 |
| A、实验Ⅱ、Ⅴ无现象,而Ⅳ生成白色沉淀,说明增大c(Mg2+)不能向生成沉淀的方向移动,增大氨水溶液的浓度才能向生成沉淀的方向移动 |
| B、实验Ⅲ无现象,因为氯化镁溶液和氨水浓度都增大,则导致氯化铵浓度增大,而氢氧化镁可以溶解在氯化铵溶液中 |
| C、由于氢氧化镁可以溶解在氯化铵溶液中,而氯化镁溶液和氨水反应可以生成氯化铵,所以该两种溶液混合后可能会出现先生成沉淀后溶解的现象 |
| D、实验Ⅲ的现象是生成白色沉淀,因为增大两种溶液中任意一种的浓度,都能使混合液的离子积达到氢氧化镁的Ksp |