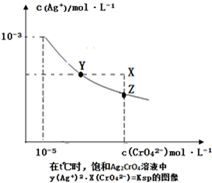
 已知t℃时AgCl的Ksp=4×10-l0,在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法错误的是( )
已知t℃时AgCl的Ksp=4×10-l0,在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法错误的是( )| A、在t℃时,Ag2CrO4的Ksp为1×10-11 |
| B、在饱和溶液中加入K2CrO4可使溶液由Y点到Z点 |
| C、在t℃时,Ag2CrO4(s)+2Cl-(aq)?2AgCl(s)+CrO42-(aq)平衡常数K=6.25×107 |
| D、在t℃时,以0.001mol/L AgNO3溶液滴定20mL 0.001mol/L KCl和0.001mol/L的K2CrO4的混和溶液,CrO42-先沉淀 |
气体A、B分别为0.6mol和0.5mol,在0.4L密闭容器中发生反应:3A+B?aC+2D,经5min后,此时C为0.2mol,又知在此反应时间内,D的平均反应速率为0.1mol?(L?min)-1,下列结论正确的是( )
| A、此时,反应混合物总的物质的量为1mol |
| B、B的转化率为50% |
| C、A的平均反应速率为0.1mol?(L?min)-1 |
| D、a值为2 |
一定温度下,关于PH=1的醋酸溶液的下列说法中正确的是( )
| A、加入等体积的水,c(H+)、c(OH-)都减小 |
| B、加水稀释时醋酸和水的电离度都增大 |
| C、加入少量醋酸钠固体pH 一定降低 |
| D、稀释100倍pH变为3 |
一定温度下,体积为2L的密闭容器中X、Y、Z三种气体的初始物质的量和平衡物质的量如表:下列说法正确的是( )
| 物质 | X | Y | Z |
| 初始物质的量(mol) | 0.2 | 0.2 | 0 |
| 平衡物质的量(mol) | 0.1 | 0.05 | 0.1 |
| A、反应可表示为2X+3Y?2Z,其平衡常数为8000 |
| B、增大压强使平衡向生成Z的方向移动,平衡常数增大 |
| C、若将容器的体积压缩至1L,则X的体积分数减小,浓度增大 |
| D、若升高温度时,Z的浓度增大,可知温度升高时正反应速率增大,逆反应速率减小,平衡朝正反应方向移动 |
某浓度的氨水中存在下列平衡:NH3?H2O?NH4++OH-,如想增大NH4+的浓度,而不增大OH-的浓度,下列措施不正确的是( )
| A、加少量MgCl2 |
| B、加入NH4Cl固体 |
| C、适当升高温度 |
| D、加入少量盐酸 |
下列化合物属于弱电解质的是( )
| A、醋酸 |
| B、Ba(OH)2 |
| C、CO2 |
| D、HF |
下列关于pH=3的盐酸和醋酸溶液的说法正确的是( )
| A、两种溶液中由水电离出来的c(H+)不相同 |
| B、中和相同体积的两种酸溶液所需NaOH的物质的量相同 |
| C、加入等质量的铁粉,反应过程中放出H2的速率相同 |
| D、分别用蒸馏水稀释m倍和n倍,两溶液pH仍相同,则m<n |
pH=1的两种一元酸HX与HY溶液,分别取50mL加入足量的镁粉,充分反应后,收集到H2体积分别为V(HX)和V(HY).若V(HX)>V(HY),则下列说法正确的是( )
| A、HX可能是强酸 |
| B、HX的酸性比HY的酸性弱 |
| C、两酸的浓度大小[HX]<[HY] |
| D、pH=1的两种一元酸均稀释100倍,稀释后两溶液的pH均为3 |
在相同的温度下,100mL 0.01mol?L-1醋酸溶液与10mL 0.1mol?L-1醋酸溶液相比较,下列数值中前者大于后者的是( )
| A、中和时所需氢氧化钠的物质的量 |
| B、H+的物质的量浓度 |
| C、电离平衡常数K |
| D、H+的物质的量 |