电解CuSO4溶液时,要求达到三点(1)阳极质量减少;(2)阴极质量增加;(3)电解质溶液中c(Cu2+)不变,则可选用的电极是( )
| A、纯铜作阳极,含Zn和Ag的铜合金作阴极 |
| B、含Zn和Ag的铜合金作阳极,纯铜作阴极 |
| C、用纯铁作阳极,纯铜作阴极 |
| D、用石墨作阳极,纯铜作阴极 |
已知25℃时,电离常数Ka(HF)=3.6×10-4 mol?L-1,溶度积常数Ksp(CaF2)=1.46×10-10.现向1L浓度均为 0.2mol?L-1 的HF和NaF溶液中加入1L 0.2mol?L-1 CaCl2溶液(忽略体积变化),则下列说法中,正确的是( )
| A、25℃时,0.1 mol?L-1 HF溶液中pH=1 |
| B、Ksp(CaF2)随温度和固体质量的变化而变化 |
| C、该体系中没有沉淀产生 |
| D、在原HF和NaF混合液中,2c(Na+)=c(F-)+c(HF) |
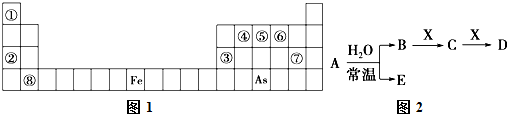
如图是元素周期表的一部分,下列说法中正确的是( )


| A、元素④、⑦、⑨的单质的氧化性依次减弱,所以在水溶液中④的单质可以置换出⑦、⑨的单质 |
| B、因为氢键关系,气态氢化物的稳定性③大于⑥ |
| C、元素⑤的单质与元素②的最高价氧化物对应的水化物反应时,参加反应的⑤单质与生成氢气的物质的量之比为2:3 |
| D、离子半径:⑥>⑦>③>④>⑤ |
下列各组离子能大量共存且溶液颜色为无色的是( )
| A、Na+、MnO4-、K+、NO3-、SO32- |
| B、Na+、CO32-、Cl-、Al3+、NO3- |
| C、Na+、S2-、OH-、K+、Cl-、NO3- |
| D、Fe2+、H+、Na+、Ca2+、NO3- |
若溶液中由水电离产生的c(OH-)=1×10-12 mol?L-1,满足此条件的溶液中一定可以大量共存的离子组是( )
| A、Al3+ Na+ NO3- Cl- |
| B、K+ Na+ Cl- NO3- |
| C、K+ Na+ Cl- CO32- |
| D、K+ NH4+ SO42- NO3- |
如图所示,装置在常温下工作(溶液体积变化忽略不计).闭合K,灯泡发光.下列叙述中不正确的是( )
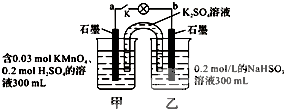

| A、当电路中有1.204×1022个电子转移时,乙烧杯中溶液的C(H+)约为0.1mol?L-1 |
| B、电池工作时,盐桥中的K+移向甲烧杯 |
| C、电池工作时,外电路的电子方向是从a到b |
| D、乙池中的氧化产物为SO42- |