海洋中有丰富的食品、矿产、能源和药物.如图是从海水中提取某些原料的流程图.下列有关说法正确的是( )


| A、从海水中提取物质都必须通过化学反应才能实现 |
| B、第②步属于物理变化 |
| C、从第④~⑤步的目的是浓缩、富集溴单质 |
| D、第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入试剂的顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
用NA表示阿伏加德罗常数,下列说法中正确的是( )
| A、2 L 0.1 mol?L-1 K2SO4溶液中离子所带电荷总数约为0.6 NA |
| B、标准状况下,22.4 L任意比的氢气和氯气的混合气体中含有的原子总数均为2NA |
| C、1 mol Cl2变为Cl-时得到的电子数为NA |
| D、由质量守恒定律可知1mol的氯化铁能形成NA个氢氧化铁胶体粒子 |
下列说法正确的是( )
①用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
②物质的溶解度随温度的升高而增加,物质的溶解都是吸热的;
③对于Al(OH)3(s)?Al(OH)3(aq)?Al3++3OH-,前者为溶解平衡,后者为电离平衡;
④除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3小;
⑤沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全.
①用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
②物质的溶解度随温度的升高而增加,物质的溶解都是吸热的;
③对于Al(OH)3(s)?Al(OH)3(aq)?Al3++3OH-,前者为溶解平衡,后者为电离平衡;
④除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3小;
⑤沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全.
| A、①②③④⑤ | B、② |
| C、①③④⑤ | D、①②⑤ |
下列对沉淀溶解平衡的描述不正确的是( )
| A、用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小 |
| B、物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的 |
| C、除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3大 |
| D、沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全 |
下列溶液中氯离子浓度最大的是( )
| A、1L1mol/LAlCl3溶液中 |
| B、2L1mol/LFeCl3溶液中 |
| C、1L2mol/LKCl溶液中 |
| D、2L3mol/LMgCl2溶液中 |
只用试管和胶头滴管,不用其它试剂无法区分的一组溶液是( )
| A、KOH溶液和AlCl3溶液 |
| B、Na2CO3溶液和盐酸 |
| C、NaHCO3溶液和NaOH溶液 |
| D、盐酸和NaAlO2溶液 |
 如图,从A处通入纯净的Cl2,打开B阀时,C处的红色布条看不到明显现象;关闭B阀后,C处红布逐渐褪色.则D瓶中装的是( )
如图,从A处通入纯净的Cl2,打开B阀时,C处的红色布条看不到明显现象;关闭B阀后,C处红布逐渐褪色.则D瓶中装的是( )| A、浓H2SO4 |
| B、NaOH溶液 |
| C、H2O |
| D、Na2S溶液 |
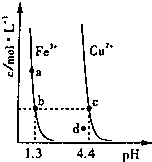 某温度下,Fe(OH)3(s)和Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图.线上任何一点表示的状态均为金属离子Mn+、OH-、M(OH)n(s)的平衡状态.据图分析,下列判断错误的是
某温度下,Fe(OH)3(s)和Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图.线上任何一点表示的状态均为金属离子Mn+、OH-、M(OH)n(s)的平衡状态.据图分析,下列判断错误的是( )
| A、Ksp[Fe(OH)3]>Ksp[Cu(OH)2] |
| B、c、d两点代表的溶液中c(H+) 与c(OH-)乘积相等 |
| C、d点所代表的Cu(OH)2溶液达到了饱和 |
| D、向含有相同浓度Fe3+和Cu2+的混合溶液中逐滴滴加NaOH溶液,先形成Fe(OH)3沉淀 |
实验室需要配制2mol/l的NaCl溶液450ml,配制时应选用的容量瓶的规格和称取的NaCl质量分别是( )
| A、450ml,52.65g |
| B、任意规格,52.65g |
| C、500 ml,58.5g |
| D、1000 ml,117g |
