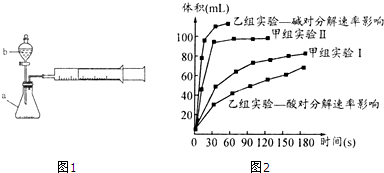
已知:Na2S2O3+H2SO4=S↓+SO2+H2O+Na2SO4,某同学通过不同温度,析出硫的快慢,来研究温度对反应速率的影响.该学生采用的研究方法是( )
①假说法
②实验法
③分类法
④比较法.
①假说法
②实验法
③分类法
④比较法.
| A、①、② | B、①、③ |
| C、②、④ | D、②、③ |
 一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=-lg c(M),pCO32-=-lg c(CO32-).下列说法不正确的是( )
一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=-lg c(M),pCO32-=-lg c(CO32-).下列说法不正确的是( )| A、MgCO3、CaCO3、MnCO3 的Ksp依次减小 |
| B、a 点可表示MnCO3 的饱和溶液,且c(Mn2+)=c(CO32-) |
| C、b 点可表示的CaCO3不饱和溶液,且c(Ca2+)<c(CO32-) |
| D、c 点可表示MgCO3 的不饱和溶液,且c(Mg2+)<c(CO32-) |
一定温度和压强下,N2(g)和H2(g)反应生成2molNH3(g),放出92.4kJ热量.在相同温度下,向一恒压容器中通入 1molN2和3molH2,达平衡时放出热量为Q1kJ;向另一体积相同恒容容器中通入1molN2和3molH2,相同温度下达到平衡时放出热量为Q2kJ.则下列叙述正确的是( )
| A、Q2>Q1=92.4kJ |
| B、Q2=Q1=92.4kJ |
| C、Q2<Q1<92.4kJ |
| D、Q2=Q1<92.4kJ |
已知4种无机化合物在水中和液氨中的溶解度(g/100g溶剂)为:
由此溶解度可知在水溶液中上述化合物发生复分解反应为:2AgNO3+BaCl2=2AgCl↓+Ba(NO3)2,那么上述几种化合物在液氨溶液中发生复分解反应的化学方程式( )
| 物质 | AgNO3 | Ba(OH)2 | AgCl | BaCl2 |
| 水中 | 216 | 9.02 | 35.8 | |
| 液氨 | 86 | 97.2 | 0.8 | 0 |
| A、2AgNO3+BaCl2=2AgCl↓+Ba(NO3)2 |
| B、2AgNO3+BaCl2=2AgCl+Ba(NO3)2↓ |
| C、2AgCl+Ba(NO3)2=2AgNO3↓+BaCl2 |
| D、2AgCl+Ba(NO3)2=2AgNO3+BaCl2↓ |
氢氧化镁悬浊液存在下列平衡:Mg(OH)2(s)
Mg2+(aq)+2OH-(aq),下列有关说法不正确的是( )
| A、加少量水,更多的氢氧化镁溶解 |
| B、加少量NaOH(s),氢氧化镁的溶解量减少 |
| C、加少量氯化氢,溶液的pH变大 |
| D、加少量MgCl2(s),溶液的pH变小 |
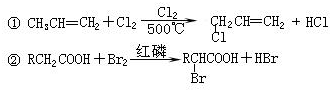
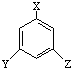 ,又能发生银镜反应,遇FeCl3溶液又能呈紫色的同分异构体有
,又能发生银镜反应,遇FeCl3溶液又能呈紫色的同分异构体有