下列实验操作或实验所得出的结论正确的是( )
A、 实验室中浓硝酸应保存在棕色细口瓶中,并贴有如图所示标签 |
| B、制备Fe(OH)3胶体时,应向沸水中逐滴加入1mol?L-1的FeCl3溶液,并继续加热到液体呈透明的红褐色为止 |
| C、用托盘天平称取5.85g NaCl,称量时砝码放在右盘,氯化钠放在左盘 |
| D、用50mL量筒量取5.6mL浓硫酸 |
| E、用四氯化碳萃取碘水中的碘,分液时有机层从分液漏斗的下端放出 |
| F、用广泛pH试纸测得某溶液的pH为4.8 |
认识危险品标志非常重要.装运浓硫酸的包装箱上应贴的图标是( )
A、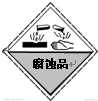 |
B、 |
C、 |
D、 |
我国稀土资源丰富,下列有关稀土元素
Sm与
Sm的说法不正确的是( )
| ||
| 62 |
| ||
| 62 |
| A、它们互为同位素 |
| B、它们是不同种核素 |
| C、它们的质量数相同 |
| D、它们的核外电指数相同 |
价电子排布为5s25p1的元素,在周期表中的位置是( )
| A、第四周期第ⅤA族 |
| B、第五周期第ⅢA族 |
| C、第五周期第ⅠA族 |
| D、第四周期第ⅢA族 |
在酸性高锰酸钾溶液中加入Na2O2粉末,高锰酸钾溶液会褪色,其中发生反应的离子方程式为:2MnO4-+16H++5Na2O2═2Mn2++5O2↑+8H2O+10Na+,下列判断正确的是( )
| A、Na2O2既是氧化剂,又是还原剂 |
| B、反应的氧化产物只有O2 |
| C、当反应产生标准状况下2.24LO2时,转移的电子为0.1mol |
| D、向高锰酸钾溶液中滴加浓盐酸可以得到酸性高锰酸钾溶液 |
下列离子方程式书写正确的是( )
| A、氢氧化钡与硫酸铜溶液反应:Ba2++SO42-=BaSO4↓ |
| B、二氧化硅与氢氧化钠溶液反应:SiO2+2OH-=SiO32-+H2O |
| C、溴化亚铁溶液中通入足量氯气:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
| D、氯化铝溶液与过量氨水反应:Al3++4NH3?H2O=AlO2-+2H2O+4NH4+ |
下列方程式书写正确的是( )
| A、HCO3-的电离方程式:HCO3-+H2O═H2CO3+OH- |
| B、NH3?H2O的电离方程式:NH3?H2O?NH4++OH- |
| C、CO32-的水解方程式:CO32-+2H2O?H2CO3+2OH- |
| D、NH4Cl的水解方程式:NH4++H2O═NH3?H2O+H+ |
下列化学方程式或离子方程式正确的是( )
A、H2S在过量的O2中燃烧:2H2S+O2
| ||||
| B、向稀HNO3中加入过量的铁:Fe+4H++NO3-═Fe3++NO↑+2H2O | ||||
| C、向稀NH4HSO3溶液中滴加足量的稀NaOH溶液:NH4++OH-=NH3?H2O | ||||
| D、向氯化铝溶液滴加过量的氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
若反应aA(g)+bB(g)?cC(g)+dD(g)△H在密闭容器内达到化学平衡后,升高温度或增大压强都会使平衡混合物中C的质量分数降低,下列关于该反应的正确说法是( )
| A、△H>0 |
| B、a+b<c+d |
| C、温度升高,平衡常数增大,平衡向逆反应方向移动 |
| D、增加A的量,平衡向正反应方向移动,A的转化率提高 |