已知:(1)H2(g)+O2(g)═H2O(g)△H1=a kJ?mol-1
(2)2H2(g)+O2(g)═2H2O(g)△H2=b kJ?mol-1
(3)H2(g)+O2(g)═H2O(l)△H3=c kJ?mol-1
(4)2H2(g)+O2(g)═2H2O(l)△H4=d kJ?mol-1
下列关系式中正确的是 ( )
(2)2H2(g)+O2(g)═2H2O(g)△H2=b kJ?mol-1
(3)H2(g)+O2(g)═H2O(l)△H3=c kJ?mol-1
(4)2H2(g)+O2(g)═2H2O(l)△H4=d kJ?mol-1
下列关系式中正确的是 ( )
| A、a<c<0 |
| B、b>d>0 |
| C、2a=b<0 |
| D、2c=d>0. |
在2L容器中发生3A+B═2C的反应,最初加入的A、B都是4mol,10s 内A的反应速率为0.12mol/(L?s),10s后容器内的B的物质的量为( )
| A、1.6 mol |
| B、2.8 mol |
| C、3.2 mol |
| D、3.6 mol |
下列有关说法正确的是( )
| A、25℃101kPa时,CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-Q kJ/mol,则甲烷的燃烧热为Q kJ/mol |
| B、CaCO3(s)=CaO(s)+CO2(g) 室温下不能自发进行,说明该反应的△H<0 |
| C、反应N2(g)+3H2(g)?2NH3(g)△H<0达到平衡后,升高温度,反应速率v(H2)和H2的平衡转化率均增大 |
| D、已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(Q1、Q2的值均大于零): H2(g)+Cl2(g)=2HCl(g)△H1=-Q1 kJ/mol H2(g)+Br2(g)=2HBr(g)△H2=-Q2 kJ/mol 则△H1<△H2 |
下列说法正确的是( )
| A、放热反应都是自发的,吸热反应都是非自发的 |
| B、自发反应一定是熵增大,非自发反应一定是熵减少或不变 |
| C、△H<0,△S>0的反应一定是自发反应 |
| D、△H>0,△S>0的反应低温时是自发反应 |
汽车燃油不完全燃烧时产生CO2有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g)△H>0,小明学完“化学反应的方向”后,认为该反应不可能实现,最合理的解释是( )
| A、该反应是熵减小反应 |
| B、该反应是吸热反应 |
| C、该反应需要和高的温度 |
| D、该反应是熵减小,烙增加的反应 |
在2A(g)+3B(g)=C(g)+4D(g)的反应中,下列表示该反应的化学反应速度最快的是( )
| A、v (A)=0.5 mol/(L?s) |
| B、v (B)=0.9 mol/(L?s) |
| C、v (C)=0.8 mol/(L?s) |
| D、v (D)=1.0 mol/(L?s) |
氢气是人类最理想的能源.已知在25℃、101kPa下,1g氢气完全燃烧生成液态水时放出热量142.9kJ,今有如下三个热化学方程式下列关于它们的表述正确的是?( )
(1)H2(g)+
O2(g)=H2O(g)△H1=a kJ?mol-1??
(2)H2O(l)=H2(g)+
O2(g)△H2=b kJ?mol-1??
(3)2H2(g)+O2(g)=2H2O(l)△H3=c kJ?mol-1??
(1)H2(g)+
| 1 |
| 2 |
(2)H2O(l)=H2(g)+
| 1 |
| 2 |
(3)2H2(g)+O2(g)=2H2O(l)△H3=c kJ?mol-1??
| A、2b=c |
| B、b=285.8? |
| C、a=-b? |
| D、氢气的燃烧热为a kJ?mol-1 |
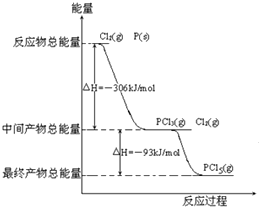 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如下图所示(图中的△H表示生成1mol产物的数据). 根据上图回答下列问题:
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如下图所示(图中的△H表示生成1mol产物的数据). 根据上图回答下列问题: