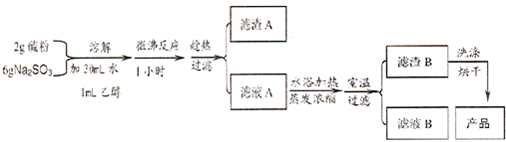
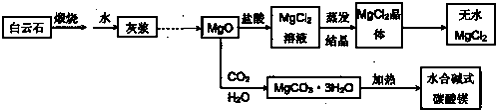
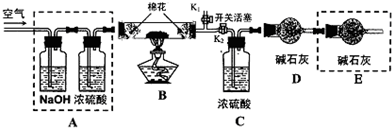
下列离子方程式书写正确的是( )
| A、铝粉投入到NaOH溶液中:2Al+2OH-=2AlO2-+H2↑ |
| B、NaAlO2溶液中加入过量盐酸:AlO2-+H++H2O=Al(OH)3↓ |
| C、NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| D、Al2O3粉末溶于NaOH溶液中:Al2O3+2OH-=2AlO2-+H2O |
设NA为阿伏加德岁常数,下列叙述正确的是( )
| A、1L 0.1 mol?L-1碳酸钠溶液中的阴离子总数为0.1NA |
| B、将400 mL 1 mol/L的HNO3溶液与7 g Fe粉充分反应,转移电子数为0.375NA |
| C、标准状况下,14 g氮气中共用电子对的数目为1.5NA |
| D、已知反应N2(g)+3H2(g)?2NH3(g)△H=-91.8KJ/mol中反应物的转化率为30%,相同条件下,当放出91.8 kJ热量时,生成氨分子的数目为0.6NA |

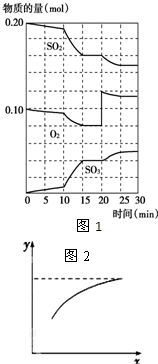 硫酸生产中,接触室内的反应为:
硫酸生产中,接触室内的反应为: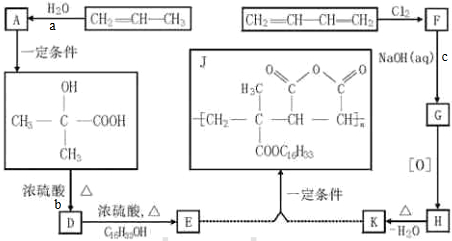
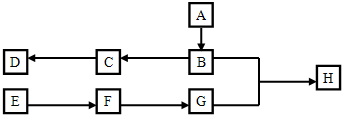
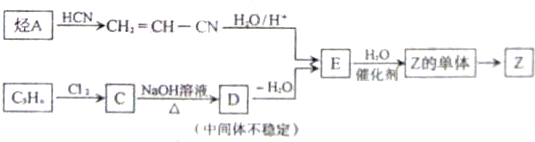

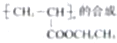 实验,此实验过程涉及的反应类型有
实验,此实验过程涉及的反应类型有