下列叙述正确的是( )
| A、用热的纯溶液清洗油污的原理可表示为:CO3 2-+H2O?HCO3-+OH- |
| B、0.1 mol?L-1的NaHCO3溶液中:K+、Al 3+、Fe3+、NO3- 可大量存在 |
| C、室温下,某溶液中只含有Al 3+、K+、NO3-、SO4 2-,则该溶液由水电离出的c(H+ )=10-13 mol?L-1 |
| D、可以用加热蒸干并充分灼烧的方法得到CuCl2溶液的溶质固体 |
把物质的量均为0.1mol的AlCl3、CuCl2和H2SO4溶于水制成100mL的混合溶液,用石墨做电极电解,并收集两电极所产生的气体,一段时间后两极收集到的气体在相同条件下体积相同.则下列描述正确的是( )
| A、电路中共转移0.9mol电子 |
| B、阳极得到的气体中有O2且其物质的量为0.35mol |
| C、阴极质量增加3.2g |
| D、若改用铜棒做电极电解该溶液,电极反应不变 |
常温下,在20mL0.1mol?L-1Na2CO3溶液中逐渐滴入0.1mol?L-1HCl溶液40mL,溶液的PH逐渐降低,下列说法正确的是( )
| A、完全反应以后,溶液呈现中性 |
| B、当盐酸加入10mL时,溶液中:c(CO32-)=C(HCO3-) |
| C、在20mL0.1mol?L-1Na2CO3溶液中:c(H+)+2c(H2CO3)+c(HCO3-)=c(OH-) |
| D、当盐酸加入20mL时,溶液中:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) |
二氧化钛(TiO2)是一种用途广泛的化工原料,用四氯化钛(TiCl4)与某常见物质X反应可制得二氧化钛,反应的化学方程式为:TiCl4+□X=TiO2+4HCl,关于物质X下列说法正确的是( )
| A、该物质由碳、氢、氧三种元素组成 |
| B、该物质的化学式为H2O2 |
| C、该物质中氢、氧元素的质量比1:8 |
| D、该物质中氢元素的质量分数为5% |
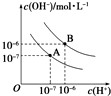 已知水在25℃(A)和T℃(B)时,其电离平衡曲线如图所示:
已知水在25℃(A)和T℃(B)时,其电离平衡曲线如图所示: