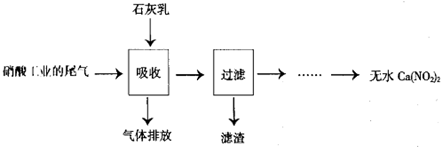
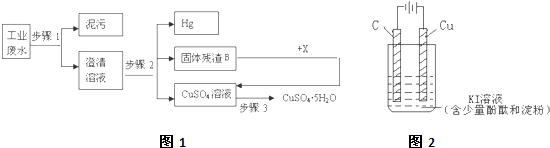
对于固定体积的密闭容器中进行的气体反应可以说明A(g)+B(g)?C(g)+D(g)在恒温下已达到平衡的是( )
| A、反应容器的压强不随时间而变化 |
| B、A气体和B气体的生成速率相等 |
| C、A、B、C三种气体的生成速率相等 |
| D、反应混合气体的密度不随时间而变化 |
下列实验设计方案,可行的是( )
| A、检验CO32-,可取少量试剂滴加稀盐酸,若产生无色无味的气体能使澄清石灰水变浑浊,则说明原溶液中一定有CO32- |
| B、检验SO42-,可取少量试剂滴加氯化钡溶液,若产生白色沉淀,则说明原溶液中有SO42- |
| C、用氢氧化钠溶液可除去CO2气体中的HCl气体 |
| D、为除去粗盐中的Ca2+、Mg2+、SO42-可依次加入过量的BaCl2、NaOH、Na2CO3后过滤,再加入适量的稀盐酸 |
一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验.某研究性学习小组在实验中配制1mol?L-1的稀硫酸标准,然后用其滴定某未知浓度的氢氧化钠溶液.下列有关说法中正确的是( )
| A、实验中所用到的锥形瓶和容量瓶,在洗涤后均需要润洗 |
| B、酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,最终氢氧化钠溶液浓度将偏大 |
| C、滴定时,左手提酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视滴定管内液面变化 |
| D、中和滴定时,若在最后一次读数时俯视读数,则导致实验结果偏大 |
常温下,有甲、乙两份体积为1L、浓度均为0.1mol.?L-1的醋酸溶液,其pH为3,①甲用蒸馏水稀释100倍后,溶液的pH变为x; ②乙与等体积、浓度为0.2mol?L-1的NaOH混合,在混合液中:n(CH3COO-)+n(OH-)-n(H+)=y mol.x、y的正确答案组合为( )
| A、3;0.1 |
| B、5;0.2 |
| C、3<x<5;0.1 |
| D、3<x<5;0.2 |
在一密闭容器中有如下反应:aX(g)+bY(g)?nW(g)△H,某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:其中,φ(W)表示W在反应混合物中的体积分数,t表示反应时间.当其他条件不变时,下列分析正确的是( )
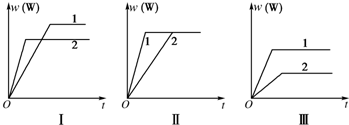
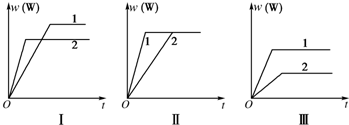
| A、图Ⅰ可能是不同压强对反应的影响,且p1>p2,a+b<n |
| B、图Ⅱ可能是不同压强对反应的影响,且p1>p2,n<a+b |
| C、图Ⅱ可能是在同温同压下不同催化剂对反应的影响,且1使用的催化剂效果好 |
| D、图Ⅲ可能是不同温度对反应的影响,且T1>T2,△H<0 |