温度为T℃时,向2.0L恒容密闭容器中充入1.0mol PCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经一段时间后达到平衡.反应过程中测定的部分数据见下表:下列说法正确的是( )
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A、反应在前50 s的平均速率为v(PCl3)=0.0032 mol?L-1?s-1 |
| B、T℃时,该反应的平衡常数为0.025 |
| C、保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol?L-1,则反应的△H<0 |
| D、相同温度下,向容器中再充入1.0 mol PCl5,达到平衡时,PCl5的转化率大于20% |
可逆反应2A(g)+3B(g)?2C(g);△H=-QkJ?mol-1(Q>0).现有甲、乙两个容积相同且不变的真空密闭容器,向甲容器中加入2molA和3molB,在一定条件下达到平衡时放出热量为Q1kJ;在相同的条件下,向乙容器中加入2molC达到平衡后吸收热量为Q2 kJ;已知2Q1=Q2.下列叙述正确的( )
| A、平衡时甲、乙中C的体积分数甲>乙 |
| B、平衡时甲中A的转化率为60% |
| C、达到平衡后,再向乙中加入0.8molA+1.2molB+1.2molC,平衡向生成A的正向移动 |
| D、D甲容器达到平衡后,升温,反应的平衡常数增大 |
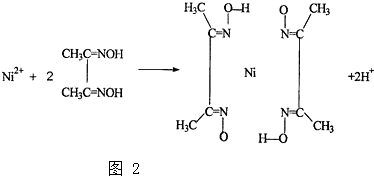
 现有8种元素,它们的原子序数依次增大,其中A、B、C、D、E为短周期主族元素,F、G、H为第四周期元素.请根据下列相关信息,回答问题.
现有8种元素,它们的原子序数依次增大,其中A、B、C、D、E为短周期主族元素,F、G、H为第四周期元素.请根据下列相关信息,回答问题.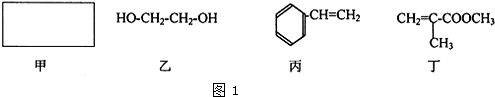

 ):又当苯环上连卤原子时,高温高压下可以水解.
):又当苯环上连卤原子时,高温高压下可以水解.


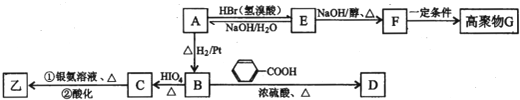
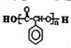 的合成路线流程图(无机试剂任选,限用4步完成).合成路线流程图如图:
的合成路线流程图(无机试剂任选,限用4步完成).合成路线流程图如图: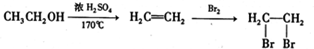

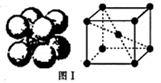
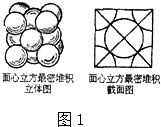 (1)现有以下几种物质::①晶体二氧化硅②干冰③五氯化磷④金刚石⑤过氧化钠⑥冰⑦碳化硅⑧白磷;请用编号填写:通过非极性键形成原子晶体的是
(1)现有以下几种物质::①晶体二氧化硅②干冰③五氯化磷④金刚石⑤过氧化钠⑥冰⑦碳化硅⑧白磷;请用编号填写:通过非极性键形成原子晶体的是