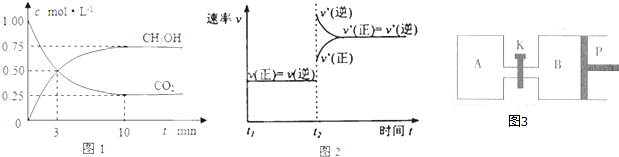
恒温下将1molN2和3mol H2 在体积为2L的容器中混合,发生如下反应:N2(g)+3H2(g)?2NH3(g),2s后测得NH3的体积分数为25%,则下列说法中不正确的是( )
| A、用N2浓度的减少表示的平均反应速率为0.2mol?L-1?s-1 |
| B、2s时N2的转化率为40% |
| C、2s时混合气体中n(N2):n(H2):n(NH3)═3:9:4 |
| D、2s时NH3的浓度为0.4mol/L |
在1100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g)?Fe(s)+CO2(g)△H=a kJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是( )
| A、若生成1molFe,则放出a kJ热量 |
| B、若升高温度,则正反应速率加快,逆反应速率减慢,化学平衡正向移动 |
| C、若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| D、达到化学平衡状态时,若c(CO)=0.100 kJ/mol,则c(CO2)=0.0263 kJ/mol |
固体粉末X中可能含有Fe、Fe2O3、K2SiO3、K2SO3、KAlO2、MgCl2、K2CO3中的若干种.为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如下:根据上述实验,以下说法正确的是( )
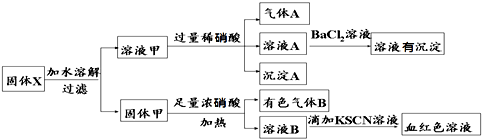

| A、气体A一定只是NO |
| B、由于在溶液A中加入BaCl2溶液有沉淀产生,因此可以判断溶液中含有K2SO3 |
| C、若向固体甲中加入足量浓盐酸,再加KSCN溶液,没有血红色,则证明原混合物中一定没有Fe2O3 |
| D、溶液甲中一定含有K2SiO3、可能含有KAlO2、MgCl2 |
水的电离平衡曲线如图所示,下列说法正确的是( )
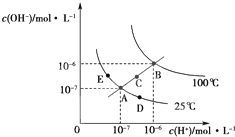

| A、图中五点KW间的关系:B=C=A=D=E |
| B、若处在B点时,将pH=2的硫酸与pH=10的KOH溶液等体积混合,溶液显酸性 |
| C、若从A点到C点,可采用:温度不变在水中加入适量的NH4Cl固体 |
| D、若从A点到D点,可采用:温度不变在水中加入少量的酸 |
下列各组离子在溶液中能够大量共存,当溶液中c(H+)=10-1mol/L时,有气体产生;而当溶液中c(H+)=10-13mol/L时,又能生成沉淀.则该组离子可能是( )
| A、Na+、Ba2+、NO3-、CO32- |
| B、Ba2+、K+、Cl-、NO3- |
| C、Mg2+、NH4+、SO42-、Cl- |
| D、Fe2+、Na+、SO42-、NO3- |
下列离子在溶液中能大量存在的( )
| A、K+、MnO4-、Cl-、H+ |
| B、AlO2-、Na+、Al3+、Cl- |
| C、Fe2+、SO42-、Cl-、Na+ |
| D、H+、AlO2-、Na+、Cl- |
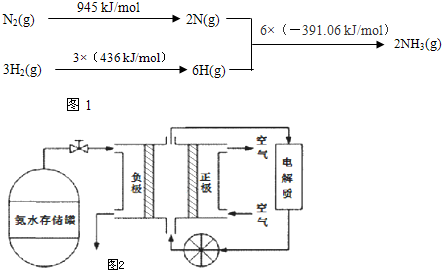
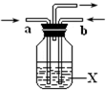 A、B、C、D、E、F、G、H是相对分子质量依次增大的气体,它们均由短周期元素组成,具有如下性质:
A、B、C、D、E、F、G、H是相对分子质量依次增大的气体,它们均由短周期元素组成,具有如下性质: