配制一定物质的量浓度的NaOH溶液时,造成实验结果偏低的原因是( )
| A、容量瓶中原有少量蒸馏水 |
| B、称量药品时间过长 |
| C、定容时俯视液面 |
| D、洗涤烧杯和玻棒的溶液转入容量瓶中 |
用98%的浓H2SO4(密度为1.84g/cm3)配制1mol/L的稀H2SO4 90mL,配制过程中需用仪器的先后顺序是( )
①20mL量筒 ②10mL量筒 ③50mL烧杯 ④托盘天平 ⑤100mL容量瓶 ⑥胶头滴管 ⑦玻璃棒.
①20mL量筒 ②10mL量筒 ③50mL烧杯 ④托盘天平 ⑤100mL容量瓶 ⑥胶头滴管 ⑦玻璃棒.
| A、①③⑤⑥⑦ |
| B、②③⑦⑤⑥ |
| C、②⑤⑦⑥① |
| D、④③⑦⑤⑥ |
某密闭容器中发生如下反应:X(g)+3Y(g)?2Z(g);△H<0.如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是( )
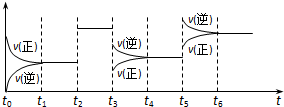

| A、t5时增大了压强 |
| B、t3时降低了温度 |
| C、t2时加入了催化剂 |
| D、t4~t5时间内转化率一定最低 |
在容积不变的密闭容器中存在如下反应2SO2(g)+O2(g)?2SO3(g)△H<0,某研究小组探究其他条件下不变时,改变某一条件对上述反应的影响,下列分析正确的是( )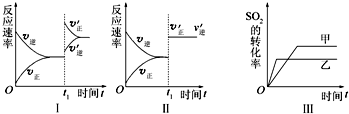

| A、图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响 |
| B、图Ⅱ表示的是t1时刻加入催化剂后对反应速率的影响 |
| C、图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙的高 |
| D、图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高 |
由两种金属组成的合金50g与氯气完全反应后,得到121g产物,则该合金的可能组成是( )
| A、Na、Zn |
| B、Na、Al |
| C、Fe、Mg |
| D、Zn、Cu |
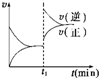 如图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或增大压强,速率的变化都符合示意图的反应是( )
如图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或增大压强,速率的变化都符合示意图的反应是( )| A、2SO2(g)+O2(g)?2SO3(g)△H< |
| B、4 NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0 |
| C、H2(g)+I2(g)?2HI(g)△H>0 |
| D、2 NH3(g)?N2(g)+3H2(g)△H>0 |
标准状况下22.4LH2 和C2H4的混合气体在一定条件下反应,所得气态物质完全燃烧恢复至常温后放出736KJ热量,混合气体中H2和C2H4的物质的量之比应为[已知H2、C2H4、C2H6的燃烧热(单位:KJ/mol)分别是286、1411和1560]( )
| A、1:3 | B、2:3 |
| C、3:1 | D、3:2 |
 空气中SO2含量是重要的空气质量指标.在工业生产上规定:空气中二氧化硫的最大允许排放浓度不得超过0.02mg?Lˉ1
空气中SO2含量是重要的空气质量指标.在工业生产上规定:空气中二氧化硫的最大允许排放浓度不得超过0.02mg?Lˉ1