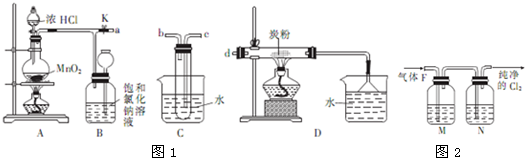
在密闭容器中进行如下反应:H2(g)+I2(g)?2HI(g),在温度T1和T2时,产物的量与反应时间的关系如图所示,符合图示的正确判断是( )
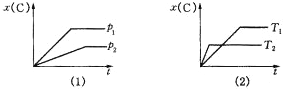
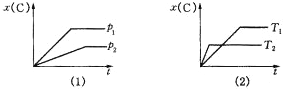
| A、T1>T2,△H>0 |
| B、T1>T2,△H<0 |
| C、T1<T2,△H>0 |
| D、T1<T2,△H<0 |
已知图一表示的是可逆反应CO(g)+H2(g)?C(s)+H2O(g)△H>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)?N2O4(g)△H<0的浓度(c)随时间(t)的变化情况.下列说法中正确的是( )
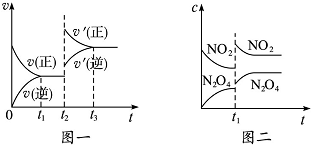

| A、图一t2时改变的条件可能是升高了温度或增大了压强 |
| B、图一t2时改变的条件一定是增大了反应物的浓度 |
| C、图二t1时改变的条件可能是升高了温度或增大了压强 |
| D、若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将减小 |
25℃时,下列各溶液中有关物质的量浓度关系正确的是( )
| A、pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合:c(Na+)+c(H+)>c(OH-)+c(CH3COO-) |
| B、Na2CO3溶液中:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、NH4HSO4溶液中滴加NaOH溶液至溶液恰好呈中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
| D、pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaOH溶液:c(CH3COONa)>c(Na2CO3)>c(C6H5ONa )>c(NaOH ) |
密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g)?2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时同的变化如图所示.下列说法中不正确是( )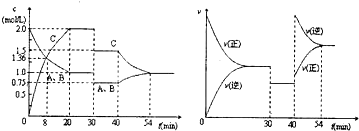

| A、该反应可以表示为A(g)+B(g)?2C(g),△H>0 |
| B、从反应开始到40min,反应物B的转化率为62.5% |
| C、30min后研究的是压强对反应速率和化学平衡的影响,40min后则是温度的影响 |
| D、在20min-30min,30min-40min的反应的平衡常数相等 |
运用元素周期律分析下面的推断正确的是( )
| A、硒化氢是无色、有毒、比硫化氢稳定的气体 |
| B、砹单质是一种有色固体,砹化氢很不稳定,砹化银是难溶于水的白色沉淀 |
| C、硫酸锶难溶于水,但易溶于盐酸 |
| D、铍(Be)是一种轻金属,它的氧化物的水化物可能具有两性 |
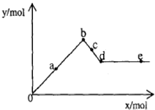 已知Ba(AlO2)2可溶于水.如图表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加人Ba(OH)2的物质的量x的关系.
已知Ba(AlO2)2可溶于水.如图表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加人Ba(OH)2的物质的量x的关系.说明:AlO2-即[Al(OH)4]-下列有关叙述正确的是( )
| A、a-b时沉淀的物质的量:A1(OH)3比BaSO4多 |
| B、c-d时溶液中离子的物质的量:AlO2-比Ba2+多 |
| C、a-d时沉淀的物质的量:BaSO4可能小于A1(OH)3 |
| D、d-e时溶液中离子的物质的量:整个阶段Ba2+一定不会等于OH- |