0 131536 131544 131550 131554 131560 131562 131566 131572 131574 131580 131586 131590 131592 131596 131602 131604 131610 131614 131616 131620 131622 131626 131628 131630 131631 131632 131634 131635 131636 131638 131640 131644 131646 131650 131652 131656 131662 131664 131670 131674 131676 131680 131686 131692 131694 131700 131704 131706 131712 131716 131722 131730 203614
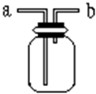 如图所示是中学化学实验中常见的装置,它有多种用途.
如图所示是中学化学实验中常见的装置,它有多种用途.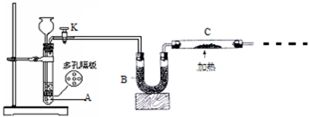 某化学课外活动小组拟用Zn和稀H2SO4制取H2还原CuO,实验装置如图.
某化学课外活动小组拟用Zn和稀H2SO4制取H2还原CuO,实验装置如图.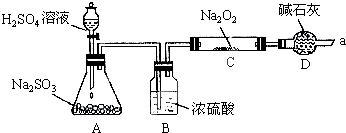
 得出结论:产物是Na2SO4,该方案是否合理
得出结论:产物是Na2SO4,该方案是否合理
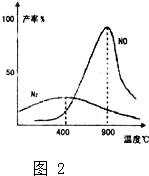
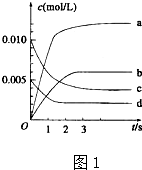 (1)在1L密闭容器内,800℃时发生反应:2NO(g)+O2(g)?2N02(g)△H<0,容器内各物质的浓度变化如图1所示.
(1)在1L密闭容器内,800℃时发生反应:2NO(g)+O2(g)?2N02(g)△H<0,容器内各物质的浓度变化如图1所示.