下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
| A、将NaHCO3固体加入新制氯水中,有无色气泡(H+) |
| B、使红色布条退色(HCl) |
| C、向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈红色(Cl2) |
| D、滴加AgNO3溶液生成白色沉淀(Cl-) |
某温度下,在一个2L的密闭容器中,加入4molA和2molB进行如下反应:3A(g)+2B(g)?4C(?)+2D(?),反应一段时间后达到平衡,测得生成1.6molC,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )
A、该反应的化学平衡常数表达式是K=
| ||
| B、此时,B的平衡转化率是35% | ||
| C、增大该体系的压强,平衡向右移动,化学平衡常数 | ||
| D、增加C,B的平衡转化率不变 |
下列有关用途的说法中,错误的是:( )
| A、液态钠可用作核反应堆的传热介质 |
| B、在过渡元素中找寻半导体材料 |
| C、考古时利用l4C测定一些文物的年代 |
| D、SiO2是制造水泥、人造宝石、单晶硅的原料 |

 有A、B、C、D、E、F六种短周期元素,其元素特征信息如表:
有A、B、C、D、E、F六种短周期元素,其元素特征信息如表: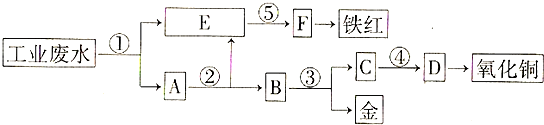
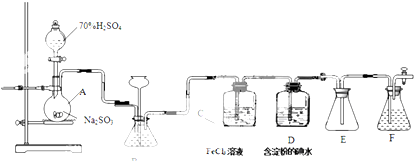
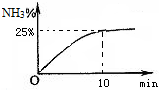 含氮化合物对人类生活有十分重大的意义.
含氮化合物对人类生活有十分重大的意义.