两种金属混合物30g,投入足量的稀盐酸中,反应后生成气体0.5mol,则混合物中的两种金属为( )
| A、镁与铁 | B、铝与铁 |
| C、镁与铝 | D、镁与锌 |
可逆反应mA(固)+nB(气)?cC(气)+fD(气)反应过程中,当其它条件不变时,C的体积分数(C%)与温度(T)和压强(P)的关系如下图所示,下列叙述正确的是( )
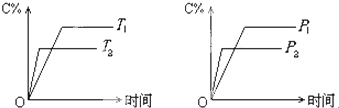

| A、达到平衡后,若使用催化剂,C的体积分数增大 |
| B、达到平衡后,若使温度升高,化学平衡向逆反应方向移动 |
| C、化学方程式中n>c+f |
| D、达到化学平衡后,增加A的量有利于化学平衡向正反应方向移动 |
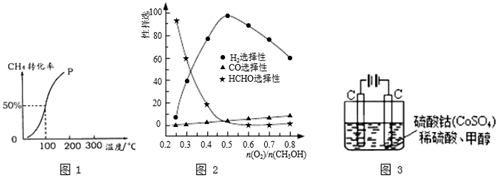
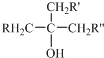 中的-OH不能被氧化.
中的-OH不能被氧化.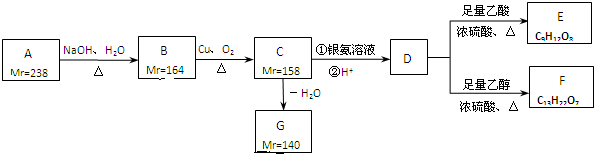
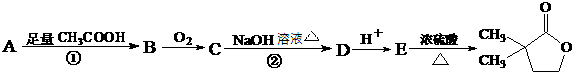
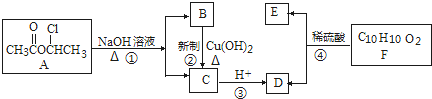
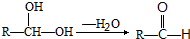 :请回答下列问题:
:请回答下列问题: