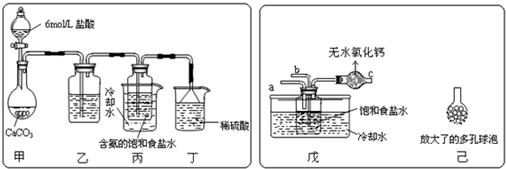
有甲、乙、丙三种溶液,进行如下操作:

则甲、乙、丙三种溶液可能是( )

则甲、乙、丙三种溶液可能是( )
| A、BaCl2、H2SO4、MgCl2 |
| B、CaCl2、HNO3、AgNO3 |
| C、CaCl2、HNO3、NaCl |
| D、BaCl2、HCl、Na2SO4 |
某溶液,只可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、NO2-、CO32-、NO3-,现取两份200mL溶液进行如下实验:(已知HNO2不稳定极易分解2HNO2=H2O+NO2↑+NO↑)
①第一份加足量AgNO3溶液后,有11.68g白色沉淀产生,沉淀中加入足量稀盐酸充分反应,有棕色气体产生,沉淀颜色不变,但是质量减少0.2g;
②将产生的气体全部通入过量的澄清石灰水,又得到白色沉淀2.0g,该沉淀能溶于稀盐酸产生无色气体;
③第二份加入过量浓NaOH溶液,加热使产生的气体全部放出,用100mL0.5mol?L-1的稀硫酸恰好完全吸收,酸也不剩余.根据上述实验,以下推测不正确的是( )
①第一份加足量AgNO3溶液后,有11.68g白色沉淀产生,沉淀中加入足量稀盐酸充分反应,有棕色气体产生,沉淀颜色不变,但是质量减少0.2g;
②将产生的气体全部通入过量的澄清石灰水,又得到白色沉淀2.0g,该沉淀能溶于稀盐酸产生无色气体;
③第二份加入过量浓NaOH溶液,加热使产生的气体全部放出,用100mL0.5mol?L-1的稀硫酸恰好完全吸收,酸也不剩余.根据上述实验,以下推测不正确的是( )
| A、原溶液一定不存在较大浓度的H+、Mg2+ |
| B、原溶液确定含NH4+、NO2-、CO32-,且物质的量之比为5:2:1 |
| C、不能确定原溶液是否含有K+、NO3- |
| D、实验中产生的棕色气体遇空气颜色会加深 |
某溶液中存在的离子有Na+、H+、S2-、HS-、OH-,则下列有关该溶液的叙述错误的是( )
| A、离子浓度可能是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+) |
| B、组成该溶液的溶质只能是Na2S或NaHS或二者的混合物 |
| C、离子物质的量的关系是2n(S2-)+n(HS-)+n(OH-)=n(Na+)+n(H+) |
| D、该溶液可能呈中性、碱性或酸性 |
下列物质中,只含有氯分子的是( )
| A、液氯 | B、盐酸 | C、氯水 | D、漂白粉 |
化学反应中,条件的有无对有些反应来说非常重要.例如,氯仿在正常情况下是一种良好的有机溶剂.能与乙醇、乙醚等多种有机溶剂互溶.但在高温、与明火或红热物体接触时,产生剧毒的光气、氯化氢等气体.光照在某些反应中也是极其重要的.在下列反应中,光照对反应几乎没有影响的是( )
| A、氯气与氢气的反应 |
| B、氯气与甲烷的反应 |
| C、氟气与氢气的反应 |
| D、次氯酸的分解 |
 品红溶液
品红溶液 溴水
溴水 澄清石灰水
澄清石灰水
 现有原子序数依次增大的A、B、C、D、E、F、G七种前36号元素.已知A、B组成的10个电子4核分子X,能使湿润的红色石蕊试纸变蓝,A、B还能组成18个电子6核分子Y;C原子的最外层电子书是次外层电子书的3倍;D、E、F三原子的最外电子层中共有10个电子,这三种元素的最高价氧化物的水化物之间,两两皆能反应且均生成盐和水;G原子核电子排布中未成对电子数在前36号元素原子钟最多.
现有原子序数依次增大的A、B、C、D、E、F、G七种前36号元素.已知A、B组成的10个电子4核分子X,能使湿润的红色石蕊试纸变蓝,A、B还能组成18个电子6核分子Y;C原子的最外层电子书是次外层电子书的3倍;D、E、F三原子的最外电子层中共有10个电子,这三种元素的最高价氧化物的水化物之间,两两皆能反应且均生成盐和水;G原子核电子排布中未成对电子数在前36号元素原子钟最多.