下列说法错误的是( )
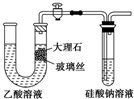

| A、使用如图所示装置验证Ka(CH3COOH)>Ka(H2CO3)>Ka(H2SiO3) |
| B、0.1 mol?L-1的醋酸中加入水或加入冰醋酸均可使平衡向电离方向移动 |
| C、等物质的量浓度的CH3COONa和Na2CO3溶液,后者溶液中水的电离程度大 |
| D、等pH的醋酸和碳酸,分别加水稀释后溶液的pH仍相等,则醋酸中加入水的体积少 |
已知25℃,醋酸溶液中存在下述关系:K=
=1.75×10-5,则有关K的下列说法正确的是( )
| c(H+)?(CH3COO-) |
| c(CH3COOH) |
| A、当向该溶液中加入一定量的硫酸时,K值增大 |
| B、升高温度,K值增大 |
| C、向醋酸溶液中加水,K增大 |
| D、向醋酸溶液中加氢氧化钠,K增大 |
在溶液中能大量共存且溶液无色的一组离子是( )
| A、Mg 2+SO42- OH- K+ |
| B、Cu2+ NO3- Cl- H+ |
| C、H+ Na+ Cl- SO42- |
| D、K+ H+ Cl- OH- |
将纯水加热至较高温度,下列叙述正确的是( )
| A、水的离子积变大、pH变小、呈酸性 |
| B、水的离了积不变、pH不变、呈中性 |
| C、水的离子积变小、pH变大、呈碱性 |
| D、水的离子积变大、pH变小、呈中性 |
下表是常温下某些一元弱酸的电离常数:物质的量浓度均为0.1mol?L-1的下列溶液中,pH由大到小的顺序是( )
| 弱酸 | HCN | HF | CH3COOH | HNO2 |
| 电离常数 | 6.2×10-10 | 6.8×10-4 | 1.8×10-5 | 6.4×10-4 |
| A、HCN>HNO2>CH3COOH>HF |
| B、HF>HNO2>CH3COOH>HCN |
| C、HCN>CH3COOH>HNO2>HF |
| D、HCN>CH3COOH>HF>HNO2 |
下列关于容量瓶使用的叙述中,正确的是( )
| A、为了使所配溶液浓度均匀,定容结束后,手握瓶颈左右振荡 |
| B、用蒸馏水洗后必须要将容量瓶烘干 |
| C、为了操作简便,浓溶液稀释可直接在容量瓶中进行 |
| D、使用前要检查容量瓶是否漏液 |
在含有Ba2+、Ca2+、Ag+的酸性溶液中,可能存在的阴离子是( )
| A、SO42- |
| B、NO3- |
| C、Cl- |
| D、CO32- |
某液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是( )
| A、K+、Na+、HCO3-、NO3- |
| B、Na+、SO42-、Cl-、ClO- |
| C、H+、Mg2+、SO42-、NO3- |
| D、Fe3+、NO3-、SCN-、Na+ |
室温时下列各组离子在指定溶液中,一定能大量共存的是( )
①无色溶液中:K+、Cl-、Na +、SO42- ②在pH=11的溶液中:Na+、AlO2-、K+、CO32-
③水电离的c (H+)=10-12mo1/L的溶液中:Cl-、HCO3-、NH4+、SO32-
④加人Al能放出H2的溶液中:Mg2+、NH4+、Cl-、SO42-
⑤pH=1的溶液中:Fe2+、Ag+、NO3-、I-.
①无色溶液中:K+、Cl-、Na +、SO42- ②在pH=11的溶液中:Na+、AlO2-、K+、CO32-
③水电离的c (H+)=10-12mo1/L的溶液中:Cl-、HCO3-、NH4+、SO32-
④加人Al能放出H2的溶液中:Mg2+、NH4+、Cl-、SO42-
⑤pH=1的溶液中:Fe2+、Ag+、NO3-、I-.
| A、①②④ | B、①②⑤ |
| C、①②③④⑤ | D、①② |