下列分离或提纯物质的方法正确的是( )
| A、用蒸馏的方法制取蒸馏水 |
| B、用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 |
| C、用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 |
| D、粗盐提纯中用加热、蒸发的方法可以除去CaCl2、MgCl2等杂质 |
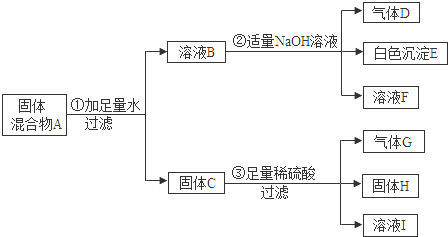
今有一混合无色澄清的水溶液,只可能含有以下离子中的若干种:Cu2+、NH4+、Cl-、
Ca2+、Ba2+、K+、CO32-、SO42-,现取三份10mL溶液进行如下实验:
①第一份加入AgNO3溶液有白色沉淀产生
②第二份加足量NaOH溶液,加热后会收集到气体
③第三份加足量BaCl2溶液后,得沉淀6.27g,经足量盐酸洗涤、干燥,沉淀质量为2,.33g.根据上述实验,以下推测正确的是( )
Ca2+、Ba2+、K+、CO32-、SO42-,现取三份10mL溶液进行如下实验:
①第一份加入AgNO3溶液有白色沉淀产生
②第二份加足量NaOH溶液,加热后会收集到气体
③第三份加足量BaCl2溶液后,得沉淀6.27g,经足量盐酸洗涤、干燥,沉淀质量为2,.33g.根据上述实验,以下推测正确的是( )
| A、NH4+、SO42-一定存在 |
| B、该溶液中含CO32-离子的浓度为1 mol/L |
| C、Cl-一定存在 |
| D、Ba2+一定不存在,Cu2+、Ca2+可能存在 |
向某溶液中加入过量盐酸生成白色沉淀,过滤后向滤液中加入过量的氢氧化钠溶液,又有白色沉淀生成;再过滤后向滤液中加入碳酸钠溶液,又生成白色沉淀,原溶液中含有的离子可能是( )
| A、Cu2+、Ba2+、Ag+ |
| B、Ag+、Ba2+、Fe3+ |
| C、Ag+、Ba2+、Mg2+ |
| D、Fe2+、K+、Ba2+ |
检验某未知溶液中是否含有SO42-,下列操作最合理的是( )
| A、加入盐酸酸化,将可能出现的沉淀过滤后,再加入Ba(NO3)2溶液 |
| B、先加入HNO3溶液酸化,再加入Ba(NO3)2溶液 |
| C、加入盐酸酸化的Ba Cl2溶液 |
| D、加入盐酸酸化,将可能出现的沉淀过滤后,再加入Ba Cl2溶液 |
要从BaCl2、NaCl的混和溶液中分别得到纯净的BaCl2和 NaCl晶体,在一系列的操作中应选用的试剂是( )
| A、K2CO3、稀盐酸 |
| B、Na2CO3、稀盐酸 |
| C、Na2CO3、稀硫酸 |
| D、NaOH、稀盐酸 |
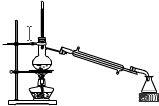 现有A、B两种有机物的液态混合物,如果A、B互溶,且相互不发生化学反应,在常压下,A的沸点为35℃,B的沸点为200℃.回答下列问题:
现有A、B两种有机物的液态混合物,如果A、B互溶,且相互不发生化学反应,在常压下,A的沸点为35℃,B的沸点为200℃.回答下列问题: