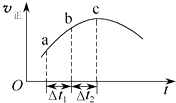
 向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)?SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( )
向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)?SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( )| A、反应物的总能量低于生成物的总能量 |
| B、反应物浓度:a点小于b点 |
| C、△t1=△t2时,SO2的转化率:a~b段小于b~c段 |
| D、反应在c点达到平衡状态 |
已知下列热化学方程式:①Zn(s)+
O2(g)═ZnO(s);△H1;②Hg(l)+
O2(g)═HgO(s);△H2.则反应Zn(s)+HgO(s)═Hg(l)+ZnO(s);△H3,△H3为( )
| 1 |
| 2 |
| 1 |
| 2 |
| A、△H1-△H2 |
| B、△H2-△H1 |
| C、△H1+△H2 |
| D、-(△H1+△H2) |
对于平衡体系:aA(g)+bB(g)?cC(g)+dD(g);正反应放热,有下列判断,其中正确的是( )
| A、若温度不变,容器体积扩大一倍,此时A的浓度是原来的0.45倍,则a+b>c+d |
| B、若从正反应开始,平衡时,A、B的转化率相等,则投入A、B的物质的量之比为 a:b |
| C、若平衡体系中共有气体M mol,再向其中充入bmolB,达到平衡时气体总物质的量为(M+b)mol,则a+b>c+d |
| D、若a+b=c+d,则当容器内温度上升时,平衡向左移动,容器中气体的压强不变 |
两种金属的混合粉末25g,与足量盐酸充分反应后,得到标准状况下的氢气11.2L.下列各组金属不可能的是( )
| A、Mg和Zn |
| B、Mg和Fe |
| C、A1和Na |
| D、A1和Cu |
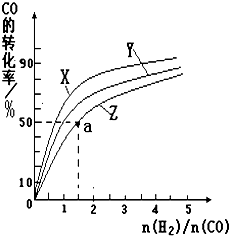 甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为: