下列有关化学实验基本知识和基本操作的描述不正确的是( )
| A、丁达尔效应可以用于区别FeCl3溶液和Fe(OH)3胶体 |
| B、加入足量浓 NaOH溶液,产生了带有强烈刺激性气味的气体.溶液中一定含有大量的NH4?+ |
| C、加入盐酸,能产生使澄清石灰水变浑浊的气体,则溶液中一定含有CO3 2- |
| D、先加入BaCl2溶液,再加入HNO3溶液,产生了白色沉淀,则溶液中一定含有大量的SO42- |
下列说法正确的是( )
| A、向2.0mL浓度均为0.lmol/L的KCl、KI混合溶液中滴加l~2滴0.01mol/LAgNO3溶液.振荡,沉淀呈黄色,说明AgCl的溶解度比AgI的溶解度小 |
| B、分别在Na2CO3和NaHCO3两种物质的溶液中,加入少量澄清石灰水,能用来鉴别这两种白色固体 |
| C、向0.1mol/L FeSO4溶液中滴加少量酸性KMnO4溶液,KMnO4溶液褪色,说明Fe2+具有氧化性 |
| D、向碘水中滴加CCl4,振荡静置后分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘 |
化学反应N2+3H2→2NH3的能量变化如图所示,该反应的热化学方程式是( )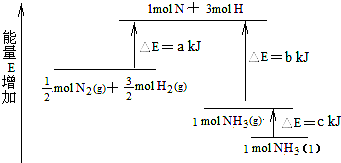
A、
| ||||
B、
| ||||
| C、N2(g)+3 H2(g)→2 NH3(g);△H=2(b-a)kJ/mol | ||||
| D、N2(g)+3 H2(g)→2 NH3(1);)△H=2(a-b-c)kJ/mol |
已知:CH4(g)+CO2(g)=2CO(g)+2H2(g);△H=+247.4kJ?mol-1.CH4(g)+H2O(g)=CO(g)+3H2(g);△H=+206.2kJ?mol-1.则CH4(g)+2H2O(g)=CO2(g)+4H2(g)的△H为( )
| A、-41.2kJ?mol-1 |
| B、+165.0kJ?mol-1 |
| C、-288.6kJ?mol-1 |
| D、+453.6kJ?mol-1 |
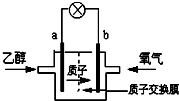 美国圣路易斯大学科学家研制了一种新型的乙醇电池(DEFC),它用磺酸类质子溶剂,在200℃左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全.电池总反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图.下列说法不正确的是( )
美国圣路易斯大学科学家研制了一种新型的乙醇电池(DEFC),它用磺酸类质子溶剂,在200℃左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全.电池总反应为:C2H5OH+3O2→2CO2+3H2O,电池示意如图.下列说法不正确的是( )| A、a极为电池的负极 |
| B、电池工作时电流由b极沿导线经灯泡再到a极 |
| C、电池正极的电极反应为:4H++O2+4e-=2H2O |
| D、1mol乙醇被氧化,电路中转移6NA个电子 |
下列说法正确的是( )
| A、难溶电解质作比较时,Ksp小的,溶解度一定小 |
| B、Ksp大小取决于难溶电解质的量,所以离子浓度改变时,沉淀平衡会发生移动 |
| C、所谓沉淀完全就是用沉淀剂将溶液中某一离子完全除去 |
| D、温度一定,当溶液中Ag+ 和Cl-浓度的乘积等于Ksp时,溶液为AgCl的饱和溶液 |
某混合溶液中可能含有下列离子中的若干种:K+、Na+、Fe2+、Fe3+、SO42-、NO2-、CO32- 现取三份20mL该溶液进行如下实验.根据上述实验,以下说法正确的是( )
①第一份加入足量稀盐酸,无任何气体产生;
②第二份加入足量NaOH,经搅拌,过滤,洗涤,灼烧,最后得到x g固体;
③第三份滴加0.1mol.L-1酸性KMnO4溶液,反应至终点,共消耗其体积为VmL;
④另用洁净的铂丝蘸取该混合溶液置于浅色火焰上灼烧,发现火焰呈现黄色.
①第一份加入足量稀盐酸,无任何气体产生;
②第二份加入足量NaOH,经搅拌,过滤,洗涤,灼烧,最后得到x g固体;
③第三份滴加0.1mol.L-1酸性KMnO4溶液,反应至终点,共消耗其体积为VmL;
④另用洁净的铂丝蘸取该混合溶液置于浅色火焰上灼烧,发现火焰呈现黄色.
| A、原混合溶液中只存在Na+、Fe3+、SO42-,不可能存在K+、CO32- |
| B、由实验①无法推断原混合溶液中是否含有SO42- |
| C、由实验①、②可判断原混合溶液中是否含有Fe3+ |
| D、由实验③可判断原混合溶液中存在Fe2+ |
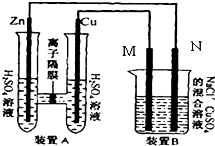 如图装置B中是浓度均为0.1mol/L的NaCl、CuSO4混合溶液,溶液体积为500ml,M、N均为石墨电极,当装置A中Zn棒质量减少6.5g时,N上质量增加
如图装置B中是浓度均为0.1mol/L的NaCl、CuSO4混合溶液,溶液体积为500ml,M、N均为石墨电极,当装置A中Zn棒质量减少6.5g时,N上质量增加