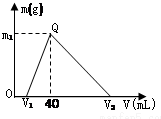
 常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到200mL c(OH-)=0.1mol/L的溶液,然后逐滴加入1mol/L的盐酸,测得生成沉淀的质量m与消耗盐酸的体积V关系如图所示,则下列说法正确的是( )
常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到200mL c(OH-)=0.1mol/L的溶液,然后逐滴加入1mol/L的盐酸,测得生成沉淀的质量m与消耗盐酸的体积V关系如图所示,则下列说法正确的是( )| A、原合金质量为 0.92 g |
| B、图中V2为 100 |
| C、整个加入盐酸过程中 Na+的浓度保持不变 |
| D、Q点m1为0.78 |
 常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到200mL c(OH-)=0.1mol/L的溶液,然后逐滴加入1mol/L的盐酸,测得生成沉淀的质量m与消耗盐酸的体积V关系如图所示,则下列说法正确的是( )
常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到200mL c(OH-)=0.1mol/L的溶液,然后逐滴加入1mol/L的盐酸,测得生成沉淀的质量m与消耗盐酸的体积V关系如图所示,则下列说法正确的是( )| A、原合金质量为 0.92 g |
| B、图中V2为 100 |
| C、整个加入盐酸过程中 Na+的浓度保持不变 |
| D、Q点m1为0.78 |