亚氯酸钠(NaClO2)可用作漂白剂,在酸性溶液中因生成亚氯酸而发生分解,分解的化学方程式为5HClO2=4ClO2↑+HCl+2H2O,ClO2是广谱型消毒剂.下列说法正确的是( )
| A、HClO2是有机酸 |
| B、上述反应中,ClO2是还原产物 |
| C、上述反应中,1 mol HClO2分解转移2 mol电子 |
| D、上述反应中,氧化剂与还原剂物质的量之比为1:4 |
下列反应的离子方程式中正确的是( )
| A、钠与水反应:2Na+2H2O=2Na++2OH-+H2↑ |
| B、氢氧化钡溶液和硫酸铵溶液反应:Ba2++SO42-=BaSO4↓ |
| C、硫化钠溶于水呈碱性:S2-+2H2O?H2S+2OH- |
| D、向溴化亚铁溶液中通入少量氯气:Cl2+2Br-=2Cl-+Br2 |
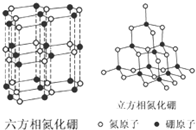 氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂,但不能导电.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.关于这两种晶体的说法,正确的是( )
氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂,但不能导电.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.关于这两种晶体的说法,正确的是( )| A、立方相氮化硼含配位键B→N |
| B、六方相氮化硼层间作用力小,所以质地软,熔点低 |
| C、两种氮化硼都属于原子晶体 |
| D、六方相氮化硼晶体其结构与石墨相似却不导电,原因是没有可以自由移动的电子 |
下列离子方程式正确的是( )
| A、向盐酸中滴加氨水:H++OH-═H2O |
| B、利用腐蚀法制作印刷线路板:Fe3++Cu═Fe2++Cu2+ |
| C、将少量Cl2通入KBr、KI的混合溶液中:Cl2+2Br-═Br2+2Cl- |
| D、向次氯酸钙溶液中通入少量的CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO |
下列说法正确的是( )
| A、二氧化碳分子中存在共价键和分子间作用力 |
| B、甲烷、氨和水都是由极性键结合而成的极性分子 |
| C、同主族不同元素的最高价氧化物,一定具有相同的晶体结构 |
| D、氟化氢的沸点高于氯化氢的沸点,正丁烷的沸点高于异丁烷的沸点 |
工业上生产下列物质,不涉及氧化还原反应的是( )
| A、用铝矾土(主要成分Al2O3)生产金属铝 |
| B、用硫铁矿(主要成分FeS2)生产硫酸 |
| C、用海水、贝壳生产氯化镁晶体 |
| D、用氯化钠生产烧碱 |
下列哪一组溶液的反应可用H++OH-=H2O 表示( )
| A、硫酸和氢氧化钡 |
| B、硫酸和烧碱 |
| C、硫酸和氢氧化铜 |
| D、硫酸和氨水 |
摩尔是( )
| A、国际单位制的一个基本物理量 |
| B、表示物质质量的单位 |
| C、表示6.02×1023个粒子的集合体 |
| D、计量微观粒子的物质的量的单位 |
制取新型水处理剂CO2的化学方程式为:2KClO3+H2C2O4+H2SO4
2ClO2+K2SO4+2CO2+2H2O.下列说法不正确的是( )
| ||
| A、KClO3在反应中得到电子 |
| B、1mol KClO3参加反应有2mol电子转移 |
| C、H2C2O4在反应中被氧化 |
| D、ClO2是还原产物 |
下列叙述中正确的是( )
| A、在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原 |
| B、有些复分解反应属于氧化还原反应 |
| C、失电子难的原子,获得电子的能力一定强 |
| D、非金属单质在氧化还原反应中可能做氧化剂也可能做还原剂 |