在化学变化中,原子结构中可能发生改变的是( )
| A、质子数 | B、中子数 |
| C、原子的核外电子数 | D、原子核 |
已知A2-离子共含有x个中子,A元素的质量数为m,则n克A2-离子共含有电子的物质的量为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
医学界通过用放射性14C标记的C60,发现一种C60的羧酸衍生物在特定条件下可通过断裂DNA杀死细胞,从而抑制艾滋病,则有关14C的叙述正确的是( )
| A、与14N 含有的中子数相同 |
| B、是C60的同素异形体 |
| C、与C60中普通碳原子的化学性质不同 |
| D、与12C互为同位素 |
已知一种混合气体由H2、N2两种气体按照体积比3:1组成,该混合气体的平均相对分子质量为( )
| A、30 | B、15 | C、34 | D、8.5 |
下列离子或原子,并非“8电子结构”的是( )
| A、Na+ |
| B、Cl- |
| C、H+ |
| D、F- |
关于反应Fe2O3+3CO
2Fe+3CO2的下列说法中正确的是( )
①Fe2O3发生氧化反应
②Fe2O3是氧化剂
③Fe是还原产物
④CO具有氧化性
⑤该反应属于置换反应.
| ||
①Fe2O3发生氧化反应
②Fe2O3是氧化剂
③Fe是还原产物
④CO具有氧化性
⑤该反应属于置换反应.
| A、②③⑤ | B、只有①② |
| C、只有②③ | D、①③④ |
下列说法正确的是( )
| A、S2-电子排布式 1s22s22p63s23p4 |
| B、在金属晶体中,自由电子与金属离子或金属原子的碰撞有能量传递,可以用此来解释的金属的物理性质是导热性 |
| C、金属键可以看做是许多原子共用许多电子所形成的强烈相互作用,所以和共价键类似,也有饱和性和方向性 |
D、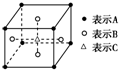 某物质的晶体中含A、B、C三种元素,其排列方式如图所示,晶胞中A、B、C的原子个数比为1:2:2. |
2010年诺贝尔化学奖授予在“钯催化交叉偶联”反应领域作出突出贡献的三位科学家,下列有关钯原子
Pd的说法错误的是( )
106 46 |
| A、质量数为106 |
| B、质子数为46 |
| C、电子数为60 |
| D、中子数为60 |
如图BF3与一定量的水形成(H2O)2?BF3晶体Q,Q在一定条件下可转化为R,反应过程中新形成的化学键包括( )


| A、离子键 | B、配位键 |
| C、金属键 | D、氢键 |
下列元素中,基态原子的外围电子排布式不正确的是( )
| A、As 4s24p3 |
| B、Cr 3d44s2 |
| C、Ar 3s23p6 |
| D、Fe 3d64s2 |