X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族,其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9,单质Y可与NaOH溶液反应生成氢气.下列说法不正确的是( )
| A、原子半径:Y>Z>W |
| B、XW2熔点为107℃,沸点为142.5℃,说明固态XW2为分子晶体 |
| C、电解YW3固体可得单质Y |
D、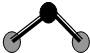 ZW2分子结构见右图,说明ZW2是极性分子 |
在氧化还原反应CuO+H2
Cu+H2O中,还原产物是( )
| ||
| A、CuO |
| B、H2 |
| C、Cu |
| D、H2O |
下列关于热化学方程式和反应的热效应的叙述中,正确的是( )
| A、已知2C(s)+2O2(g)═2CO2(g);△H1,2C(s)+O2(g)=2CO(g);△H2.则△H1<△H2 | |||
B、500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)
| |||
| C、含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应的热化学方程式为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(aq);△H=-57.4 kJ/mol | |||
| D、已知2H2(g)+O2(g)═2H2O(g);△H=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol |
元素X、Y和Z可结合形成化合物XYZ3;X、Y和Z的原子序数之和为26;Y和Z在同一周期.下列有关推测正确的是( )
| A、XYZ3是一种可溶于水的酸,且X与Y可形成共价化合物XY |
| B、XYZ3是一种微溶于水的盐,且Y与Z可形成共价化合物化合物YZ或YZ2 |
| C、XYZ3是一种易溶于水的盐,且X与Z可形成离子化合物XZ |
| D、XYZ3是一种离子化合物,且Y与Z可形成离子化合物YZ3 |
下列反应中,不属于氧化还原反应的是( )
| A、锌和硫酸反应:Zn+H2SO4═ZnSO4+H2 |
| B、碳酸钙和盐酸反应:CaCO3+2HCl═CaCl2+CO2+H2O |
| C、亚硫酸和双氧水反应:H2SO3+H2O2═H2SO4+H2O |
| D、铁和硫酸铜溶液反应:Fe+CuSO4═FeSO4+Cu |
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的是( )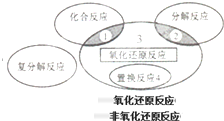

| A、4Fe(OH)2+O2+2H2O=4Fe(OH)3 | ||||
B、2NaHCO3
| ||||
C、4NH3+5O2
| ||||
| D、Zn+H2SO=ZnSO4+H2↑ |