下列物质中不含配位键的是( )
| A、NH4+ |
| B、H3O+ |
| C、KOH |
| D、Fe(SCN)3 |
下列各选项中所述的两个量,前者一定大于后者的是( )
| A、1 L 0.3 mol?L-1 CH3COOH和3 L 0.1 mol?L-1 CH3COOH中的H+数目 |
| B、1 L 0.3 mol?L-1 CH3COOH和3 L 0.1 mol?L-1 CH3COOH的电离常数 |
| C、在4NH3+6NO═5N2+6H2O反应中,被氧化和被还原的N原子数 |
| D、纯水在25℃和80℃时的pH |
下列叙述正确的是( )
| A、c(H+)等于1×10-7 mol/L的溶液一定是中性溶液 |
| B、任何浓度的溶液都可以用pH来表示其酸性的强弱 |
| C、无论是纯水、酸性、碱性或中性稀溶液,常温下,其c(H+)?c(OH-)=1×10-14 |
| D、0.2 mol/L CH3COOH溶液中的c(H+)是0.1 mol/L CH3COOH溶液中的c(H+)的2倍 |
25℃时,水的电离达到平衡:H2O?H++OH-,下列叙述正确的是( )
| A、向水中加入少量固体Na2CO3,平衡逆向移动,c(OH-)增大 |
| B、向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 |
| C、向水中加入少量固体NaOH,平衡逆向移动,c(H+)降低,KW减小 |
| D、将水加热,KW增大,pH不变 |
常温下,纯水中存在电离平衡:H2O?H++OH-.欲使水的电离平衡向正方向移动,并使c(H+)增大,应加入的物质是( )
| A、FeCl3 |
| B、H2SO4 |
| C、NaHCO3 |
| D、NaOH |
pH=13的 强碱与pH=2的强酸溶液混合,所得混合液的pH=7,则强碱与强酸的体积比为( )
| A、9:1 | B、1:9 |
| C、1:10 | D、10:1 |
关于杂化轨道的说法不正确的是( )
| A、原子中能量相近的某些轨道,在成键时能重新组合成能量相等的新轨道 |
| B、杂化轨道的数目与杂化前的轨道数目可以相等,也可以不等 |
| C、杂化轨道成键时,要满足原子轨道最大重叠原理、最小排斥原理 |
| D、杂化轨道只能用于形成σ键或容纳孤电子对 |
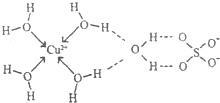 第四周期元素的单质及化合物在工农业生产中应用广泛.
第四周期元素的单质及化合物在工农业生产中应用广泛. 影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究.实验药品:铜、铁、镁、0.5mol/LH2SO4、2mol/LH2SO4、18.4mol/LH2SO4
影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究.实验药品:铜、铁、镁、0.5mol/LH2SO4、2mol/LH2SO4、18.4mol/LH2SO4