下列反应既属于化合反应又属于氧化还原反应的是( )
| A、SO2+H2O═H2SO3 | ||||
B、C+CO2
| ||||
C、H2+CuO
| ||||
D、CaCO3
|
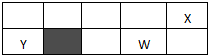 已知:X、Y、Z、W为短周期元素,原子半径X:99pm Y:154pm Z:125pm W:117pm,X、Y、W位置如图所示(副族省略),X、Y、Z的最高价氧化物对应的水化物相互能反应,下列说法正确的是( )
已知:X、Y、Z、W为短周期元素,原子半径X:99pm Y:154pm Z:125pm W:117pm,X、Y、W位置如图所示(副族省略),X、Y、Z的最高价氧化物对应的水化物相互能反应,下列说法正确的是( )| A、元素Z处于周期表的阴影位置 |
| B、X与W形成的化合物熔点很高,为离子化合物 |
| C、X、W的最高价氧化物对应水化物的酸性:X>W |
| D、Y、W的最高价氧化物的晶体类型相同 |
X、Y、Z是短周期的三种主族元素,在周期表中的相对位置如图所示,下列说法正确的是( )


| A、原子半径:X<Y<Z |
| B、X、Y、Z三种元素的最高价氧化物对应水化物中最多有一种强酸 |
| C、X的气态氢化物的稳定性比Y的气态氢化物强 |
| D、常温下X、Y、Z的单质不可能均与盐酸反应 |
下列事实,不能用勒沙特列原理解释的是( )
| A、溴水中有下列平衡Br2+H2O?HBr+HBrO 当加入AgNO3溶液后,溶液颜色变浅 |
| B、合成NH3反应,为提高NH3的产率,理论上应采取低温度的措施 |
| C、反应CO+NO2?CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动 |
| D、对2HI(g)?H2(g)+I2(g),平衡体系增大压强可使颜色变深 |
设NA为阿伏加德罗常数,下列说法不正确的是( )
| A、1mol O2与金属钠反应,O2不一定得到4NA个电子 |
| B、标准状况下,a L CH4和a L C6H14中所含分子数均为a NA/22.4 |
| C、常温常压下,1mol氯气与足量的金属镁反应,转移2NA个电子 |
| D、在20℃、1.01×105 Pa时,2.8g C2H4和CO的混合气体含气体分子数等于0.1 NA |
下列事实得出的结论正确的是( )
| A、某雨水样品放置一段时间,pH由5.6变为4.3,说明水中溶解了更多的CO2 |
| B、用一束强光照射经过煮沸的三氯化铁溶液有光的通路,说明已生成氢氧化铁胶体 |
| C、常温下铜可溶于浓硝酸,铁不溶于浓硝酸,说明铜比铁更活泼 |
| D、二氧化硫溶于水所得的溶液可导电,说明二氧化硫是电解质 |
用NA表示阿伏德罗常数,下列叙述正确的是( )
| A、标准状况下,22.4LH2O含有的分子数为NA |
| B、常温常压下,1.06gNa2CO3含有的Na+离子数为0.01NA |
| C、通常状况下,NA个CO2分子占有的体积为22.4 L |
| D、常温常压下,48gO2和O3的混合气体中含有的氧原子数为3NA |
下列说法不正确的是( )
| A、《京都议定书》针对六种温室气体进行削减,包括二氧化碳(CO2)、甲烷(CH4)、氧化亚氮(N2O)、氢氟碳化物(HFCs)、全氟碳化物(PFCs)及六氟化硫(SF6).科学研究发现,同条件下等体积的甲烷产生的温室效应远远强于二氧化碳的.那么等质量的二氧化碳产生温室效应比甲烷的强 |
| B、合成高学科王效、稳定、廉价的太阳能光电转化材料,是开发利用太阳能的关键 |
| C、稀土元素都是长周期元素,稀土资源是国家战略性资源 |
| D、环境问题的最终解决要依靠科技进步,通常利用沉淀反应除去污水中的重金属离子 |
用NA代表阿伏加德罗常数,下列说法正确的是( )
| A、物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为1 NA |
| B、标准状况下,11.2 L H2O 所含的分子数为0.5NA |
| C、常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA |
| D、18g H2O 和H2O2 的混合物含有的分子数为1NA |