为了有效除去工业食盐中的Ca2+、Mg2+、SO42-,加入试剂的合理顺序为( )
| A、先加NaOH,后加Na2CO3,再加BaCl2 |
| B、先加NaOH,后加BaCl2,再加Na2CO3 |
| C、先加BaCl2,后加NaOH,再加Na2CO3 |
| D、先加Na2CO3,后加BaCl2溶液,再加NaOH |
一定条件下,充分燃烧一定量的丁烷放出热量161.9kJ,经测定完全吸收生成的CO2需消耗5mol/L的KOH溶液100ml,恰好生成正盐,则此条件下热化学方程式:C4H10(g)+
O2(g)→4CO2(g)+5H2O(g)的△H为( )
| 13 |
| 2 |
| A、+2590.4kJ/mol |
| B、-2590.4kJ/mol |
| C、+1295.2kJ/mol |
| D、-1295.2kJ/mol |
悉尼奥运会所用火炬燃料为65%丁烷(C4H10)和35%丙烷,已知:下列有关说法正确的是( )
CO:2CO(g)+O2(g)=2CO2(g);△H=-566.0kJ/mol.
丙烷:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);△H=-2221.5kJ/mol.
正丁烷:C4H10(g)+6.5O2(g)=4CO2(g)+5H2O(l);△H=-2878.0kJ/mol.
异丁烷:C4H10(g)+6.5O2(g)=4CO2(g)+5H2O(l);△H=-2869.6kJ/mol.
CO:2CO(g)+O2(g)=2CO2(g);△H=-566.0kJ/mol.
丙烷:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);△H=-2221.5kJ/mol.
正丁烷:C4H10(g)+6.5O2(g)=4CO2(g)+5H2O(l);△H=-2878.0kJ/mol.
异丁烷:C4H10(g)+6.5O2(g)=4CO2(g)+5H2O(l);△H=-2869.6kJ/mol.
| A、常温下,正丁烷的燃烧热为-2878.0kJ/mol |
| B、相同质量的丙烷和正丁烷分别完全燃烧,前者需要的氧气多,产生的热量也多 |
| C、常温下,CO的燃烧热为566.0 kJ/mol |
| D、人类利用的能源都是通过化学反应获得的 |
一定条件下,在容积为10L的密闭容器中,将l mol X和1mol Y进行如下反应:2X(g)+Y(g)?Z(g),经60s达到平衡生成0.3mol的Z,下列说法正确的是( )
| A、60 s内X的平均反应速率为0.01 mol?L-1?s-1 |
| B、升高温度,若X的体积分数减小,则正反应的△H<0 |
| C、将容器的容积变为20 L,达平衡后Z的浓度为0.015 mol?L-1 |
| D、保持温度和体积不变,若再充入1 mol X,Y的转化率将增大 |
在一个密闭容器中发生如下反应:2SO2(g)+O2(g)═2SO3(g),反应过程中某一时刻SO2、SO3、O2的浓度分别为0.2mol?L-1,0.2mol?L-1,0.2mol?L-1,当反应达到平衡时可能的数据是( )
| A、c(SO3)=0.4 mol?L-1 |
| B、c(SO2)=c(SO3)=0.15 mol?L-1 |
| C、c(SO2)=0.4mol?L-1 |
| D、c(SO2)+c(SO3)=0.4 mol?L-1 |
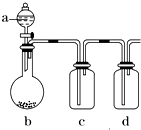 有几个实验小组的同学,利用如图装置进行“一器多用”的实验探究(a中盛放的液体均匀慢速滴下;b中盛放的药品足量;若在c、d中盛装液体,则长导管均浸入液面以下),每组同学设想在a、b、c、d中分别盛放不同物质,来制取某种气体并检验其性质.
有几个实验小组的同学,利用如图装置进行“一器多用”的实验探究(a中盛放的液体均匀慢速滴下;b中盛放的药品足量;若在c、d中盛装液体,则长导管均浸入液面以下),每组同学设想在a、b、c、d中分别盛放不同物质,来制取某种气体并检验其性质.