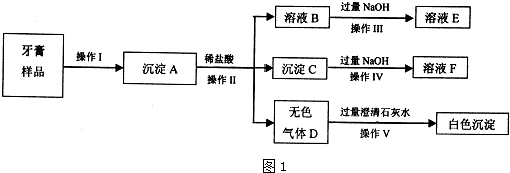
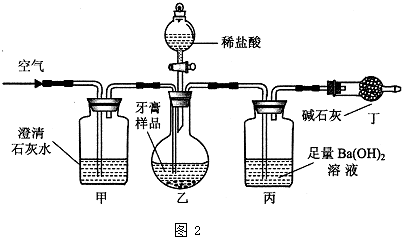
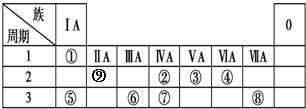
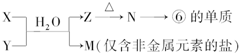对下列实验过程的评价,正确的是( )
| A、某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐 |
| B、某溶液中滴加碳酸钠溶液产生白色沉淀,说明原溶液含有Ba2+ |
| C、某无色溶液滴入紫色石蕊试液显红色,该溶液一定显碱性 |
| D、验证烧碱溶液中是否含有Cl-,先加足量的稀硝酸除去OH-,再加入AgNO3溶液,有白色沉淀,证明含Cl- |
苹果酸的结构简式为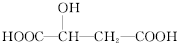 ,下列说法正确的是( )
,下列说法正确的是( )
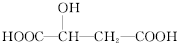 ,下列说法正确的是( )
,下列说法正确的是( )A、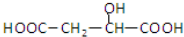 与苹果酸互为同分异构体 与苹果酸互为同分异构体 |
| B、1 mol苹果酸可与3 mol NaOH发生中和反应 |
| C、1 mol苹果酸与足量金属Na反应生成1 mol H2 |
| D、四联苯的一氯代物有5种 |
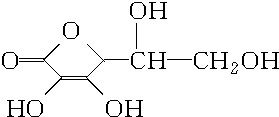 维生素C是一种水溶性维生素(其水溶液呈酸性),分子式为C6H8O6,结构如图所示.人体缺乏维生素C易得坏血病,所以维生素C又称抗坏血酸,维生素C易被空气中的氧气氧化.在新鲜的水果、蔬菜、乳制品中都含维生素C,如新鲜的橙汁中维生素C的含量在500mg?L-1左右.下列关于维生素C的叙述错误的是( )
维生素C是一种水溶性维生素(其水溶液呈酸性),分子式为C6H8O6,结构如图所示.人体缺乏维生素C易得坏血病,所以维生素C又称抗坏血酸,维生素C易被空气中的氧气氧化.在新鲜的水果、蔬菜、乳制品中都含维生素C,如新鲜的橙汁中维生素C的含量在500mg?L-1左右.下列关于维生素C的叙述错误的是( )| A、维生素C能使溴水褪色 |
| B、维生素C可作食品添加剂 |
| C、维生素C可发生酯化反应 |
| D、维生素C在碱性条件下能稳定存在 |
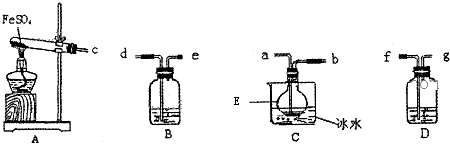
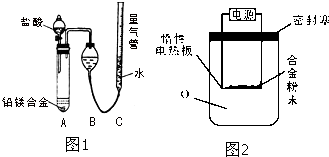 为测定某含铝95%一97%的铝镁合金(不含其它元素)中铝的质量分数,研究性学习小组的三位同学分别设计下列三种不同实验方案进行探究.填写下列空白.
为测定某含铝95%一97%的铝镁合金(不含其它元素)中铝的质量分数,研究性学习小组的三位同学分别设计下列三种不同实验方案进行探究.填写下列空白.