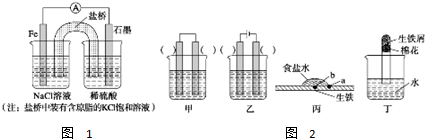
设C+CO2?2CO△H>0(吸热反应)反应速率为 v1,N2+3H2?2NH3△H<0 (放热反应)反应速率为 v2,对于上述反应,当温度升高时,v1和v2的变化情况为( )
| A、都增大 |
| B、都减小 |
| C、?v1增大,?v2减小 |
| D、?v1减小,?v2增大 |
通常情况下,NCl3是一种油状液体,其分子空间构型为NH3相似,下列对NCl3和NH3的有关叙述正确的是( )
| A、分子中N-Cl键键长与CCl4分子中C-Cl键键长相等 |
B、在氨水中,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3?H2O分子,则NH3?H2O的结构式为 |
| C、NCl3分子是非极性分子 |
| D、NBr3比NCl3易挥发 |
下列说法错误的是( )
| A、NH4NO3 溶于水虽然吸热,但其溶于水是自发过程 |
| B、加热液体(温度高于沸点)会自发转变成气体,可用熵变解释 |
| C、同温同压下,H2(g)+Cl2(g)?2HCl(g)在光照和点燃条件下的△H不同 |
| D、要正确判断化学反应能否自发进行,要综合考虑反应的△H和△S |
下列哪一项是通过降低反应所需的能量和增加活化分子的百分数来加快反应速率的( )
| A、增大物质的量浓度 |
| B、增大压强 |
| C、升高温度 |
| D、使用催化剂 |
以下自发反应可用焓判据来解释的是( )
| A、硝酸铵自发地溶于水 |
| B、2N2O5(g)═4NO2(g)+O2(g)△H=+56.7 kJ/mol |
| C、(NH4)2CO3(s)═NH4HCO3(s)+NH3(g)△H=+74.9 kJ/mol |
| D、2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol |
下面关于电解质的叙述中错误的是( )
| A、在水溶液中或熔融状态下均不导电的化合物叫非电解质 |
| B、电解质、非电解质都指化合物而言,单质不属于此范畴 |
| C、电解质在水中一定能导电,在水中导电的化合物一定是电解质 |
| D、BaSO4不溶于水,但BaSO4是电解质 |
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的( )
| A、NH4Cl |
| B、KCl溶液 |
| C、NaNO3 |
| D、CH3COONa |