下列工业生产的主要化学反应,不牵涉勒沙特列原理的是( )
| A、合成氨工业 | B、硫酸工业 |
| C、氯碱工业 | D、纯碱工业 |
下列说法正确的是( )
| A、能电离出H+的化合物叫做酸 |
| B、实验测得1mol某气体体积为22.4L,测定条件一定是标准状况 |
| C、摩尔是七个基本物理量之一 |
| D、用树状分类法可以将化合物分类为酸、碱、盐和氧化物 |
下列各组物质全部是弱电解质的是( )
| A、H2O、NH3?H2O、H3PO4、HF |
| B、Cu(OH)2、CH3COOH、C2H5OH、CH3COONa |
| C、H2SO3、Ba(OH)2、BaSO4 AgCl |
| D、H2SiO3、H2S、CO2 |
难挥发性二硫化钽(TaS2)可采用如图装置提纯.将不纯的TaS2粉末装入石英管一端,抽真空后加入适量碘并封管,置于加热炉中,发生反应:TaS2(s)+2I2(g)
TaI4(g)+S2(g).下列说法正确的是( )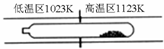
| 1123K |
| 1023K |

| A、在不同温度区域,TaI4的量保持不变 |
| B、在提纯过程中,I2的量不断减少 |
| C、该反应的平衡常数与TaI4和S2的浓度乘积成反比 |
| D、在提纯过程中,I2的作用是将TaS2从高温区转移到低温区 |
常温下,下列溶液中C(H+)最大的是( )
| A、pH=0的溶液 |
| B、0.04 mol?L-1H2SO4 |
| C、0.5 mol?L-1HCl |
| D、0.5 mol?L-1CH3COOH |
在0.1mol?L-1CH3COOH溶液中存在如下电离平衡:CH3COOH?CH3COO-+H+对于该平衡,下列叙述正确的是( )
| A、加入水时,平衡向逆反应方向移动 |
| B、加入少量NaOH固体,平衡向正反应方向移动 |
| C、通入少量HCl气体,溶液中PH值增大 |
| D、加入少量CH3COONa固体,平衡向正反应方向移动 |
下列过程需要通电才能进行的是( )
①电离 ②电镀 ③电解 ④电化学腐蚀 ⑤铜的精练.
①电离 ②电镀 ③电解 ④电化学腐蚀 ⑤铜的精练.
| A、①③④ | B、②③⑤ |
| C、①②③ | D、全部 |
下列措施或事实不是因平衡移动引起的是( )
| A、新制的氯水在光照下颜色变浅 |
| B、Fe(SCN)3溶液中加入固体KSCN后颜色变深 |
| C、H2、I2、HI平衡混合气加压后颜色变深 |
| D、在合成氨的反应中,加压有利于氨的合成 |
下列溶液中,在相同的条件下导电能力最强的是( )
| A、50mL1mol/LAlCl3 |
| B、500mL0.3mol/LFeCl3 |
| C、1.0L4mol/LNaCl |
| D、200mL3mol/LMgCl2 |