常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、滴入酚酞溶液显红色的溶液中:K+、Na+、Cu2+、SO42- |
| B、加入过量NaOH溶液或少量稀H2SO4时,都能产生白色沉淀的溶液:K+、Ba2+、Cl-、HCO3- |
| C、水电离产生的c(H+)=10-13 mol?L-1的溶液中:Na+、Cl-、NO3-、CH3COO- |
| D、pH=1的溶液中:Na+、NO3-、S2-、Cl- |
如图各装置中,均为电解液,不能构成原电池的是( )
A、 |
B、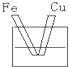 |
C、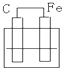 |
D、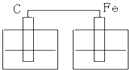 |
下列说法正确的是( )
| A、向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体,结论:NO3-被还原为NO2 |
| B、SO2能使加了酚酞的NaOH溶液褪色,加热,溶液立即再变红色 |
| C、通过摇晃试剂瓶可区分浓硫酸和稀硫酸 |
| D、浓硝酸有强氧化性,常温下能与Fe发生反应 |
红热的木炭与浓HNO3反应产生的气体经如下处理:
气体产物
气体Ⅰx mL
气体Ⅱy mL(在无氧环境下操作)假设气体体积均在相同状况下测定,不考虑气体的溶解,则x和y的关系是( )
气体产物
| 浓H2SO4干燥 |
| ①足量饱和NaHCO3溶液 |
| ②浓H2SO4干燥 |
A、x=
| ||
B、y=
| ||
| C、x=y | ||
D、y=
|
一个原电池的总反应的离子方程式是Zn+Cu2+═Zn2++Cu,该原电池的合理组成是( )
| 正极 | 负极 | 电解质溶液 | |
| A | Cu | Zn | CuSO4 |
| B | Cu | Zn | H2SO4 |
| C | Zn | Cu | CuCl2 |
| D | Mg | Zn | CuCl2 |
| A、A | B、B | C、C | D、D |
不论以何种比例混合,将甲和乙两种混合气体同时通入过量的丙溶液中,一定能产生沉淀的组合是( )
| 序号 | 甲 | 乙 | 丙 |
| ① | SO2 | CO2 | 石灰水 |
| ② | HCl | CO2 | 氢氧化钡溶液 |
| ③ | Cl2 | SO2 | BaCl2 |
| ④ | N2 | SO2 | Ba(NO3)2 |
| ⑤ | CO2 | NH3 | CaCl2 |
| A、②③④⑤ | B、①③④ |
| C、①②③④⑤ | D、①②③④ |
足量铜溶于一定量浓硝酸,产生NO2、N2O4、NO的混合气体,这些气体若与2.24LO2(标准状况)混合后通入水中,气体被水完全吸收.若向原所得溶液中加入l0mol?L-1H2SO4溶液100mL,则继续溶解的Cu的质量为( )
| A、0 | B、32g |
| C、38.4g | D、48g |
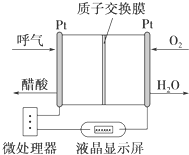 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )
如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )| A、电流由O2所在的铂电极经外电路流向另一电极 |
| B、O2所在的铂电极处发生还原反应 |
| C、该电池的负极反应式为:CH3CH2OH+3H2O-12e-═2CO2↑+12H+ |
| D、微处理器通过检测电流大小而计算出被测气体中酒精的含量 |
同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3、②NO2进行喷泉实验,经充分反应后,两瓶内溶液的物质的量浓度大小为( )
| A、①>② | B、①<② |
| C、①=② | D、不能确定 |
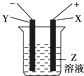 根据如图所示装置回答:
根据如图所示装置回答: