下列叙述正确的是( )
| A、向铬酸钾饱和溶液中加硫酸,溶液由黄色变为橙色 |
| B、对于可逆反应N2(g)+3H2(g)?2NH3(g)增大氮气浓度可增加活化分子百分数,从而使反应速率增加 |
| C、将AlCl3溶液和NaAlO2溶液分别蒸干后灼烧,所得固体产物均为Al2O3 |
| D、恒容密闭容器中进行的反应3A(g)?B(g)+C(g),在其它条件不变情况下,再充入一定量的A气体,A的转化率将减小 |
某温度下,在一容积可变的密闭容器里,反应2A(g)?B(g)+2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol、4mol.在保持温度和压强不变的条件下,下列说法正确的是( )
| A、充入1mol稀有气体氦(He),平衡将向正反应方向移动 |
| B、充入A、B、C各1mol,平衡将向正反应方向移动 |
| C、将A、B、C各物质的量都减半,C的百分含量变大 |
| D、加入一定量的A气体达平衡后,C的百分含量一定增加 |
一定温度下,某容积不变的密闭容器中,不能说明可逆反应:C(s)+H2O(g)?CO(g)+H2(g)在一定条件下已达到化学平衡状态的是( )
| A、v正(CO)=v逆(H2O) |
| B、体系的压强不再发生变化 |
| C、生成n mol CO的同时生成n mol H2 |
| D、1 mol H-H键断裂的同时断裂2 mol H-O键 |
在一定的温度下,可逆反应A(g)+3B(g)?2C(g)+3D(s)达到平衡的标志是( )
| A、体系中混合气体的密度保持不变 |
| B、A、B、C的浓度相等 |
| C、单位时间生成n mol A,同时分解2n mol C |
| D、A、B、C的分子数之比为1:3:2 |
下列图象不符合事实是( )
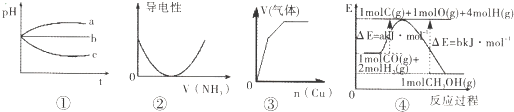

| A、图①:pH相同的H2S溶液、稀H2SO4溶液、H2SO3溶液露置于空气中一段时间后,溶液的pH随时间的变化情况 |
| B、图②:表示向乙酸溶液中通入NH3过程中溶液导电性的变化 |
| C、图③:将铜粉加入到一定量浓硝酸中产生的气体与加入铜量的变化情况 |
| D、图④知合成甲醇的热化学方程式为CO(g)+2H2(g)=CH3OH(g)△H=-(b-a)kJ?mol-1 |
氢氟酸为弱酸.250C时将0.1mol?L-1的HF加水不断稀释,下列表示的量保持不变的是( )
①n(H+); ②c(H+)?c(OH-);③c(OH-)+c(F-);④
⑤
.
①n(H+); ②c(H+)?c(OH-);③c(OH-)+c(F-);④
| c(H+) |
| c(HF) |
| c(H+).c(F-) |
| c(HF) |
| A、①③④ | B、②③④ |
| C、③④⑤ | D、②⑤ |
反应A(g)+3B(g)?2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是( )
| A、v(A)=0.15 mol/(L?min) |
| B、v(B)=0.06 mol/(L?min) |
| C、v(C)=0.04 mol/(L?s) |
| D、v(D)=0.01 mol/(L?s)) |
等质量的钠、镁、铝投入到1L 1mol/L的H2SO4中,充分反应后,放出氢气的体积分别是V1、V2、V3,则下列关系一定不正确的是( )
| A、V1>V2=V3 |
| B、V3>V2>V1 |
| C、V1>V2>V3 |
| D、V2=V3>V1 |