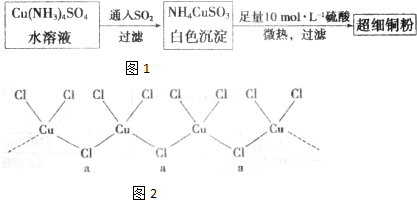
在298K、1.01×105 Pa下,将22g CO2通入750mL 1mol/L NaOH溶液中充分反应,测得反应放出x kJ的热量.已知在该条件下,1mol CO2通入1L 2mol/L NaOH溶液中充分反应放出y kJ的热量.则CO2与NaOH溶液反应生成NaHCO3的热化学方程式是( )
| A、CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2y-x)kJ/mol |
| B、CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2x-y)kJ/mol |
| C、CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(4x-y)kJ/mol |
| D、2CO2(g)+2NaOH(l)═2NaHCO3(l)△H=-(8x-2y)kJ/mol |
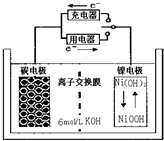 一种碳纳米管能够吸附氢气,可做二次电池(如图所示)的碳电极.该电池用6mol/L 的KOH溶液作电解质溶液,下列说法中正确的是( )
一种碳纳米管能够吸附氢气,可做二次电池(如图所示)的碳电极.该电池用6mol/L 的KOH溶液作电解质溶液,下列说法中正确的是( )| A、充电时OH-向碳电极移动 |
| B、充电时将镍电极与电的负极相连 |
| C、放电时碳电极反应为:H2-2e-=2H+ |
| D、放电时镍电极反应为:NiO(OH)+H2O+e-=Ni(OH)2+OH- |
关于如图所示的原电池,下列说法正确的是( )
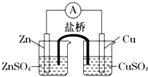

| A、锌是电池的负极,发生还原反应 |
| B、盐桥中的阳离子向硫酸铜溶液中迁移 |
| C、电流从锌电极通过检流计流向铜电极 |
| D、铜电极上发生的电极反应是2H++e-=H2↑ |
某有机化合物的结构简式为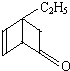 ;其中属于芳香醇的同分异构体共有( )
;其中属于芳香醇的同分异构体共有( )
 ;其中属于芳香醇的同分异构体共有( )
;其中属于芳香醇的同分异构体共有( )| A、4种 | B、5种 | C、6种 | D、8种 |
下列关于实验现象的描述不正确的是( )
| A、把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| B、用锌片做阳极,铁片做阴极,电解氯化铜溶液,铁片表面析出铜 |
| C、把铜片插入三氯化铁溶液,在铜片表面析出铁 |
| D、把锌放入稀盐酸中,加几滴氯化铜溶液,产生气泡速率加快 |
分子式为C5H12O的醇与和它相对分子质量相等的一元羧酸进行酯化反应,生成的酯共有(不考虑立体异构)( )
| A、15种 | B、16种 |
| C、17种 | D、18种 |
以葡萄糖为燃料的微生物燃料电池结构示意图如图所示.关于该电池的叙述正确的是( )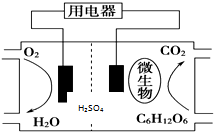

| A、该电池能够在高温下工作 | ||
| B、放电过程中,H+从正极区向负极区迁移 | ||
| C、电池的负极反应为:C6H12O6+6H2O-24e-═6CO2↑+24H+ | ||
D、在电池反应中,每消耗1 mol 氧气,理论上能生成标准状况下CO2气体
|
要证明某溶液中不含Fe3+,而可能含有Fe2+,合理的操作顺序是( )
①加入足量氯水 ②取少量试液 ③加入少量KSCN溶液.
①加入足量氯水 ②取少量试液 ③加入少量KSCN溶液.
| A、①③② | B、③②① |
| C、②③① | D、②①③ |
对于平衡体系mA(g)+nB(g)?pC(g)+qD(g);△H<0.下列结论中不正确的是( )
| A、若温度不变压强增大到原来的2倍,达到新平衡时,总体积一定比原来的1/2要小 |
| B、若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n |
| C、若m+n=p+q,则往含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a |
| D、若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则m+n<p+q |