下列热化学方程式正确的是( )
| A、2SO2+O2?2SO3;△H=-196.6 kJ?mol-1 | ||
B、H2 (g)+
| ||
| C、2H2 (g)+O2 (g)=2H2O(l);△H=-571.6 kJ | ||
| D、C(s)+O2 (g)=CO2 (g);△H=+393.5 kJ?mol-1 |
关于如图所示装置的判断,叙述正确的是( )
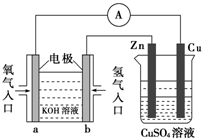

| A、左边的装置是电解池,右边的装置是原电池 |
| B、该装置中铜为正极,锌为负极 |
| C、当铜片的质量变化为12.8 g时,a极上消耗的O2在标准状况下的体积为2.24 L |
| D、装置中电子的流向是:a→Cu→经过CuSO4溶液→Zn→b |
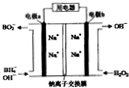 以NaBH4(B元素的化合价为+3)和H2O2为原料的电池,可以作为空军通讯卫星的高能电池.其电极负材料为Pt/C,正极材料为MnO2,其工作原理如图所示,下列说法不正确的是( )
以NaBH4(B元素的化合价为+3)和H2O2为原料的电池,可以作为空军通讯卫星的高能电池.其电极负材料为Pt/C,正极材料为MnO2,其工作原理如图所示,下列说法不正确的是( )| A、该电池工作时Na+由a极区移向b极区 |
| B、正极材料采用MnO2,MnO2既做电极材料又有催化作用 |
| C、该电池的负极反应为:BH4-+8OH--8e-→BO2-+6H2O |
| D、电路中通过6.02×1022个电子时,理论上消耗H2O2 0.1mol |
钢铁发生电化学腐蚀时,负极发生的反应是( )
| A、2H++2e-═H2 |
| B、2H2O+O2+4e-═4OH- |
| C、Fe-2e-═Fe2+ |
| D、4OH-+4e-═2H2O+O2 |
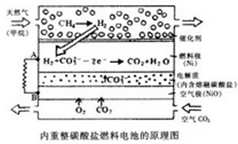 以熔融Li2CO3和K2CO3为电解质,天然气经重整催化作用提供反应气的燃料电池如图,下列说法正确的是( )
以熔融Li2CO3和K2CO3为电解质,天然气经重整催化作用提供反应气的燃料电池如图,下列说法正确的是( )| A、该电池将热能转化为电能 |
| B、外电子流动方向:由B流向A |
| C、空气极发生电极反应式为:O2+4c-+2CO2=2CO32- |
| D、以此电池为电源电解精炼铜,当有0.1mole-转移时,有3.2g铜溶解 |
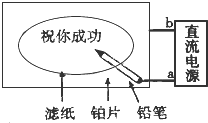 某学生设计了一个“黑笔写红字”的趣味实验,如图所示.滤纸先用氯化钠、无色酚酞的混合液浸湿,接通电源后,用铅笔在滤纸上写字,会出现红色字迹.据此,回答下列
某学生设计了一个“黑笔写红字”的趣味实验,如图所示.滤纸先用氯化钠、无色酚酞的混合液浸湿,接通电源后,用铅笔在滤纸上写字,会出现红色字迹.据此,回答下列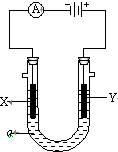 如图表示一个精炼粗铜的电解池,电解液a选用CuSO4溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
如图表示一个精炼粗铜的电解池,电解液a选用CuSO4溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: