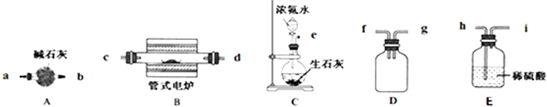
药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:下列有关叙述正确的是( )
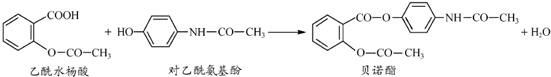

| A、贝诺酯分子中所有碳原子一定共平面 |
| B、可用FeCl3 溶液区别乙酰水杨酸和对乙酰氨基酚 |
| C、贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠 |
| D、乙酰水杨酸和对乙酰氨基酚均可与NaHCO3 溶液反应 |
某固体NaOH因吸收了空气中的CO2而含有杂质,若要将该固体配制成较纯的溶液,则其主要的实验操作过程应是( )
| A、溶解→加适量BaCl2溶液→过滤 |
| B、溶解→加适量CaCl2溶液→过滤 |
| C、溶解→加适量Ca(OH)2溶液→过滤 |
| D、溶解→加适量盐酸→加热 |
现有一瓶物质是甲和乙的混合物,已知甲和乙的某些性质如下表所示:据此,将甲和乙相互分离的最佳方法是( )
| 物质 | 熔点 | 沸点 | 密度 | 水中溶解性 |
| 甲 | -98℃ | 57.7℃ | 0.93g?cm-3 | 可溶 |
| 乙 | -84℃ | 97℃ | 0.90g?cm-3 | 可溶 |
| A、萃取法 | B、过滤法 |
| C、蒸馏法 | D、分液法 |
 用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考如图所示从下表中选出正确选项( )
用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考如图所示从下表中选出正确选项( ) | 选项 | 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 |
| A | 碱 | 酸 | 石蕊 | 甲 |
| B | 酸 | 碱 | 酚酞 | 甲 |
| C | 碱 | 酸 | 甲基橙 | 乙 |
| D | 酸 | 碱 | 酚酞 | 乙 |
| A、A | B、B | C、C | D、D |
用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液时,下列操作会引起测定结果偏高的是( )
(1)滴定时,装待测溶液的锥形瓶有少量水;(2)酸式滴定管用蒸馏水洗后,未用标准溶液洗;(3)滴定终点读数时,仰视刻度线.
(1)滴定时,装待测溶液的锥形瓶有少量水;(2)酸式滴定管用蒸馏水洗后,未用标准溶液洗;(3)滴定终点读数时,仰视刻度线.
| A、只有(1) |
| B、只有(2) |
| C、(2)(3) |
| D、(1)(2)(3) |
常温下,用0.1000mol?L-1 NaOH溶液分别滴定20.00mL 0.1000mol?L-1 盐酸和20.00mL 0.1000mol?L-1醋酸溶液,得到两条滴定曲线,如图所示,若以HA表示酸,下列说法正确的是( )
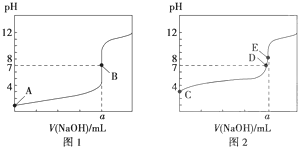

| A、滴定盐酸的曲线是图2 |
| B、达到B、E状态时,反应消耗的n(CH3COOH)>n(HCl) |
| C、达到B、D状态时,两溶液中离子浓度均为c(Na+)=c(A-) |
| D、当0mL<V(NaOH)<20.00mL时,对应混合液中各离子浓度大小顺序为c(A-)>c(Na+)>c(H+)>c(OH-) |
实验室用标准盐酸测定未知浓度NaOH溶液,用甲基橙作指示剂,下列操作可能使测定结果偏低的是( )
| A、酸式滴定管在装酸液前未用标准酸液润洗 |
| B、开始时酸式滴定管尖嘴部分留有气泡,滴定过程中消失 |
| C、锥形瓶内溶液颜色由黄变橙时立即停止滴定 |
| D、盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次 |
常温下,用0.10mol?L-1 NaOH溶液分别滴定20.00mL 0.10mol?L-1 HCl溶液和20.00mL 0.10mol?L-1CH3COOH溶液,得到2条滴定曲线,如图所示,则下列说法正确的是( )
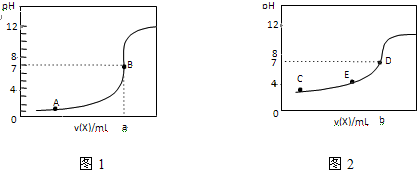

| A、图2是滴定盐酸的曲线 |
| B、a与b的关系是:a<b |
| C、E点对应离子浓度由大到小的顺序为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D、这两次滴定都可以用甲基橙作为指示剂 |